
【题目】下列离子方程式错误的是 ( )
A. CuO+2H+==Cu2++H2O B. CaCO3+2H+==Ca2++CO2↑+H2O
C. 2Fe+6H+==2Fe3++3H2↑ D. Cu(OH)2+2H+==Cu2++2H2O
科目:高中化学 来源: 题型:
【题目】下列关于物质分类的说法正确的是
A.烧碱﹑纯碱﹑碱石灰都是碱B.BaSO4﹑C2H5OH﹑氨水都是电解质
C.硝酸、硫酸、次氯酸都是酸D.CaO﹑Na2O2﹑K2O都是碱性氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合溶液中所含离子的浓度如下表,则 M 离子可能为 ( )
所含离子 | NO3- | SO42- | H+ | M |
浓度/(molL-1) | 2 | 1 | 2 | 1 |
A.Cl-B.Ba2+C.Na+D.Mg2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y两根金属棒插入Z溶液中构成如图的装置,实验中电流表指针发生偏转,同时X棒变粗,Y棒变细,则X、Y、Z可能是下列中的( )

选项 | X | Y | Z |
A | Zn | Cu | 稀硫酸 |
B | Cu | Zn | 稀硫酸 |
C | Cu | Ag | 硫酸铜溶液 |
D | Ag | Zn | 硫酸铜溶液 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室以苯甲醛为原料制备间溴苯甲醛(实验装置见下图)。其实验步骤为:
步骤1:将三颈瓶中的一定配比的无水AlCl3、1,2-二氯乙烷和苯甲醛充分混合后,升温至60℃,缓慢滴加经浓硫酸干燥过的液溴,保温反应一段时间,冷却。
步骤2:将反应混合物缓慢加入一定量的稀盐酸中,搅拌、静置、分液。有机相用10%NaHCO3溶液洗涤。
步骤3:经洗涤的有机相加入适量无水MgSO4固体,放置一段时间后过滤。
步骤4:减压蒸馏有机相,收集相应馏分。

下列说法错误的是
A. 甲同学认为步骤1中使用1,2-二氯乙烷的目的是做催化剂,加快反应速率
B. 乙同学认为可在该实验装置的冷凝管后加接一只装有无水MgSO4的干燥管,实验效果可能会更好
C. 丙同学认为步骤2中有机相使用10%NaHCO3溶液洗涤可除去大部分未反应完的Br2
D. 丁同学认为步骤4中减压蒸馏有机相是因为间溴苯甲醛高温下容易氧化或分解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1 mol/L H2SO4的含义是
A.1L 水中含有1mol H2SO4 B.1L 溶液中含有1mol H+
C.1L H2SO4溶液中含98g H2SO4 D.将98g H2SO4溶于1L水配成溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.某反应在体积为5L的恒容密闭的绝热容器中进行,各物质的量随时间的变化情况如下图所示(已知A、B、C均为气体)。
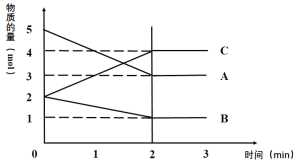
(1)该反应的化学方程式为__________________。
(2)反应开始至2分钟时,B的平均反应速率为______________。
(3)能说明该反应已达到平衡状态的是_________。
A.υ(A)=2υ(B) B.容器内气体密度不变 C.υ逆(A)=υ正(C)
D.各组分的物质的量相等 E. 混合气体的平均相对分子质量不再改变的状态
(4)由图求得平衡时A的转化率为________。
II.已知甲烷燃烧的化学反应方程式为CH4+2O2![]() CO2+2H2O,若以4mol/L 500mL KOH(aq)为电解质溶液,将其设计为原电池,则
CO2+2H2O,若以4mol/L 500mL KOH(aq)为电解质溶液,将其设计为原电池,则
(1)其正极电极方程式为___________。
(2)至某时刻溶液中c(CO32-)=1mol/L,则导线上通过的电子的物质的量为_____,此时消耗标准状况下CH4体积_____ L 。(假设化学能全部转化为电能;溶液体积保持不变)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于Li、Na、K、Rb、Cs的叙述均正确的一组是( )
①金属性最强的是铯 ②它们的氧化物都只有M20和M202两种形式
③在自然界中均以化合态形式存在 ④密度按Li→Cs 顺序依次递增
⑤离子半径:Rb+>K+>Na+
A.①②③B.③④⑤C.②④⑤D.①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质分类正确的是( )
A.Na2O2、Fe2O3、Al2O3均为碱性氧化物B.稀豆浆、硅酸溶胶、CuSO4溶液均为胶体
C.烧碱、冰醋酸、四氯化碳均为电解质D.盐酸、水玻璃、漂白液均为混合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com