
| A、Fe(OH)3中胶粒直径小于1nm |
| B、可以发生丁达尔现象 |
| C、Fe(OH)3能通过滤纸 |
| D、Fe(OH)3胶粒带正电荷 |


科目:高中化学 来源: 题型:
 如图为CO2电催化还原为碳氢化合物的工作原理示意图,用一种钾盐水溶液作电解液.下列说法不正确的是( )
如图为CO2电催化还原为碳氢化合物的工作原理示意图,用一种钾盐水溶液作电解液.下列说法不正确的是( )| A、工作时,铜片作阴极 |
| B、工作时,K+向铜片电极移动 |
| C、工作时,铂片上的电极反应式为4OH--4e-=O2↑+2H2O |
| D、若CxHy为C2H4,则生成1 mol C2H4的同时生成2 molO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、室温下,测0.1mol/L HX溶液的pH,若pH>1,证明HX是弱酸 |
| B、室温下,测1mol/L NaX溶液的pH,若pH>7,证明HX是弱酸 |
| C、将等浓度、等体积的HCl和NaX溶液混合,若混合溶液pH<7,证明HX是弱酸 |
| D、相同条件下,对0.1 mol/L的HCl和0.1 mol/L的HX进行导电性实验,若与HX溶液相串联的灯泡较暗,证明HX为弱酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
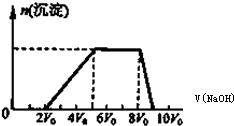 (1)双氧水能使酸性高锰酸钾溶液褪色,其反应的离子方程式如下,请将相关物质的化学计量数填写在方框里:
(1)双氧水能使酸性高锰酸钾溶液褪色,其反应的离子方程式如下,请将相关物质的化学计量数填写在方框里:| 可能大量含有的阳离子 | H+、Mg2+、Al3+、NH4+、Fe3+ |
| 可能大量含有的阴离子 | Cl-、Br-、CO32-、AlO2- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com