
 在分析化学中常用Na2C2O4晶体作为基准物质测定KMnO4溶液的浓度.在H2SO4溶液中,反应如下:2MnO4-+5C2O42-+16H+
在分析化学中常用Na2C2O4晶体作为基准物质测定KMnO4溶液的浓度.在H2SO4溶液中,反应如下:2MnO4-+5C2O42-+16H+
| ||
| W |
| 5 |
| W |
| 5 |
| 2 |
| 0.02L×c |
| 5×134 | ||
|
| 2W |
| 67 |
| 2W |
| 67 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NA个N2与0.5NA个H2物质的量之比为2:1 |
| B、标准状况下,11.2LBr2含有的原子数为NA |
| C、5.6L氯气和16.8L氧气的混合气体中所含的分子数一定为NA |
| D、1mol/LNaCl溶液中含有NA个氯离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 将洁净的三种金属片X、Y和Z分别放置在浸有食盐溶液的滤纸上并压紧(如图).每次实验时,电压表指针的偏移方向和读数如下表.已知构成两电极的金属,活泼性相差越大,则电压越大.对X、Y、Z和铜四种金属的下列说法,不正确的是( )
将洁净的三种金属片X、Y和Z分别放置在浸有食盐溶液的滤纸上并压紧(如图).每次实验时,电压表指针的偏移方向和读数如下表.已知构成两电极的金属,活泼性相差越大,则电压越大.对X、Y、Z和铜四种金属的下列说法,不正确的是( )| 金属片 | 电子流向 | 电压(V) |
| X | X→Cu | +0.78 |
| Y | Cu→Y | -0.15 |
| Z | Z→Cu | +1.35 |
| A、Z金属可作为牺牲阳极保护法的阳极,保护Y金属 |
| B、Y金属不能从硫酸溶液中置换出氢气 |
| C、三种金属的活泼性顺序为:Z>X>Y |
| D、X和Y能构成电压最大的原电池 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| H2CO3 | Ka1=4.3×10-7 | H2C2O4 | Ka1=5.6×10-2 |
| Ka2=5.6×10-11 | Ka2=5.42×10-5 |
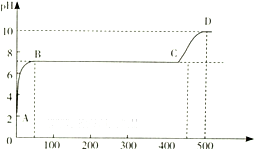
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 滴定序号 | 待测液体积∕mL | 消耗KMn04溶液体积∕mL |
| 1 | 25.00 | 19.98 |
| 2 | 25.00 | 19.12 |
| 3 | 25.00 | 20.02 |
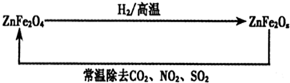
查看答案和解析>>
科目:高中化学 来源: 题型:
A、铝粉投入到NaOH溶液中:2Al+2OH-═2Al
| ||
| B、铁与盐酸反应:Fe+2H+═Fe3++H2↑ | ||
C、用小苏打治疗胃酸过多:H++HC
| ||
| D、硫酸铜溶液跟氢氧化钡溶液反应:Ba2++SO42-═BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、少量NaHSO4溶液与Ba(OH)2溶液混合:S
| ||
| B、醋酸除水垢:CaCO3+2CH3COOH=Ca2++2CH3COO-+CO2↑+H2O | ||
| C、漂白粉溶液中通入过量的CO2:Ca2++2ClO-+CO2+H2O=CaCO3↓+2HClO | ||
| D、少量金属钠放入冷水中:Na+2H2O=Na++2OH-+H2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com