
����Ŀ��������H��һ���л��������м��塣ʵ�����ɷ��㻯����A�Ʊ�H��һ�ֺϳ�·��ͼ���£�

��֪����![]()
��![]()
�ش��������⣺
��1��A�Ļ�ѧ������________________��������й�ƽ���ԭ�������____����
��2����B����C��1���ķ�Ӧ��������________________��
��3��E�Ľṹ��ʽΪ________________��
��4��F�����Ӿ۷�Ӧ�Ļ�ѧ����ʽΪ_______________________________________��
��5��G��һ�ȴ�����_______�֡�
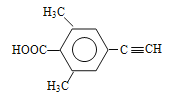
��6�����㻯����X��F��ͬ���칹�壬X�����뱥��̼��������Һ��Ӧ�ų�CO2����˴Ź���������ʾ��4�ֲ�ͬ��ѧ�������⣬�������Ϊ6:2:1:1��д������Ҫ���X�Ľṹ��ʽ_________________��
��7��д���û������2-��ȲΪԭ���Ʊ�������![]() �ĺϳ�·��ͼ___________�������Լ���ѡ����
�ĺϳ�·��ͼ___________�������Լ���ѡ����
���𰸡� ����ȩ 14 ������Ӧ 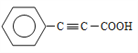
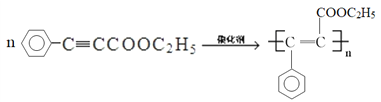 3
3 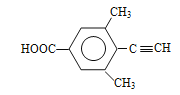 ��
�� ��
�� ��
��
������������������Ϣ�ٿ�֪��AΪ����ȩ���ṹ��ʽΪ![]() ��BΪ
��BΪ![]() ��B�����Ƶ�������ͭ�������ữ������C����CΪ
��B�����Ƶ�������ͭ�������ữ������C����CΪ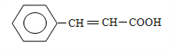 ��C���巢���ӳɷ�Ӧ����D����DΪ
��C���巢���ӳɷ�Ӧ����D����DΪ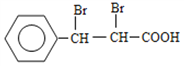 ��D������ȥ��Ӧ���ữ��õ�E����EΪ
��D������ȥ��Ӧ���ữ��õ�E����EΪ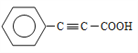 ��E���Ҵ�����������Ӧ����F����FΪ
��E���Ҵ�����������Ӧ����F����FΪ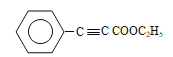 ��F��G������Ϣ�ڷ�Ӧ����H����GΪ
��F��G������Ϣ�ڷ�Ӧ����H����GΪ![]() ���ݴ˽����
���ݴ˽����
�⣺��1��A�Ľṹ��ʽΪ![]() ����ѧ�����DZ���ȩ������ȩ���ͱ�������ƽ���νṹ����������й�ƽ���ԭ�������14����
����ѧ�����DZ���ȩ������ȩ���ͱ�������ƽ���νṹ����������й�ƽ���ԭ�������14����
��2���������Ϸ�����֪��B����C��1���ķ�Ӧ��������������Ӧ��
��3��E�Ľṹ��ʽΪ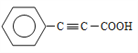 ��
��
��4��FΪ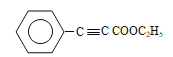 �������Ӿ۷�Ӧ�Ļ�ѧ����ʽΪ
�������Ӿ۷�Ӧ�Ļ�ѧ����ʽΪ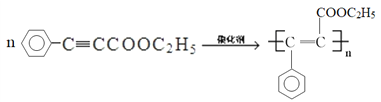 ��
��
��5��GΪ![]() �������к���3����ԭ�ӣ�G��һ�ȴ�����3�֡�
�������к���3����ԭ�ӣ�G��һ�ȴ�����3�֡�
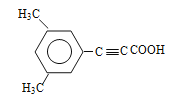
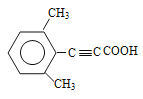
��6�����㻯����X��F��ͬ���칹�壬X���뱥��̼��������Һ��Ӧ�ų�CO2����X���������Ȼ�����˴Ź���������ʾ��4�ֲ�ͬ��ѧ�������⣬�������Ϊ6��2��1��1������Ҫ���X�Ľṹ��ʽΪ ��
�� ��
�� ��
�� ������4�֣�
������4�֣�
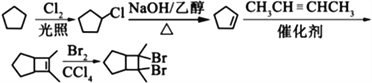
��7���û������2-��ȲΪԭ���Ʊ�������![]() ���������û��������壨���������ڹ��������·���ȡ����Ӧ����һ�廷���飨��һ�Ȼ����飩��Ȼ��һ�廷���鷢����ȥ��Ӧ���ɻ���ϩ������ϩ��2-��Ȳ������Ϣ�ڷ�Ӧ�������������巢���ӳɷ�Ӧ���ɵõ���Ʒ������ϳ�·��������
���������û��������壨���������ڹ��������·���ȡ����Ӧ����һ�廷���飨��һ�Ȼ����飩��Ȼ��һ�廷���鷢����ȥ��Ӧ���ɻ���ϩ������ϩ��2-��Ȳ������Ϣ�ڷ�Ӧ�������������巢���ӳɷ�Ӧ���ɵõ���Ʒ������ϳ�·��������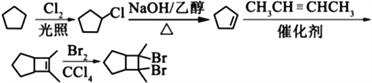 ��
��


 �»����ܶ�Ա��ϵ�д�
�»����ܶ�Ա��ϵ�д� ����ͼ����ּ��������ҵ֣�ݴ�ѧ������ϵ�д�
����ͼ����ּ��������ҵ֣�ݴ�ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�Dz��ֶ�����Ԫ�ػ��ϼ���ԭ�������Ĺ�ϵͼ������˵������ȷ����
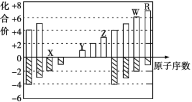
A. ��̬�⻯����ȶ��ԣ�R>W
B. X��Y�����γ�ԭ�Ӹ�����Ϊ1:1��1:2���������ӻ�����
C. ��X��Y��Z��W��R����Ԫ���γɵļ������а뾶��С����X2-
D. Y��Z��������������Ӧ��ˮ���������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ij�л��ﺬ��4��C��ÿ��Cԭ�Ӷ��Լ�����ȵ�������������3��C���������ṹ������̼̼��֮��ļнǶ�Ϊ60����������˵������ȷ����
A. ���л�����C��ȡsp2�ӻ�
B. ���л����һ�ȴ������1��
C. ���л����̼ԭ�ӹ�����������
D. ���л���IJ����Ͷ�Ϊ3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��H2S ��SO2 ��Ի��������彡�����������Σ������ҵ�ϲ�ȡ���ַ�����������Щ�к�������ŷš�
I.H2S �ij�ȥ
����1: ������H2S����Ӧ��ԭ��ΪH2S + Fe2(SO4)3==S��+2FeSO4+H2SO4��4FeSO4+O2+2H2SO4![]() 2Fe2(SO4)3 +2H2O��
2Fe2(SO4)3 +2H2O��
��1����˾�����ʱ��FeSO4����������������ʱ��5��105 �����þ���������______��
��2����ͼ1��ͼ2 �жϣ�ʹ����˾����������Ϊ_________������Ӧ�¶ȹ��ߣ���Ӧ�����½�����ԭ����______________��


����2: ��һ�������£���H2O2 ����H2S
��3�����Ųμӷ�Ӧ��n(H2O2)/n(H2S) �仯���������ﲻͬ����n(H2O2)/n(H2S)=4ʱ���������� �ķ���ʽΪ________��
II.SO2 �ij�ȥ
����1( ˫�): ��NaOH ����SO2 ������CaO ʹNaOH ����:NaOH ��Һ![]() Na2SO3
Na2SO3
��4��д�������������ӷ���ʽ:_________________��
��5��CaO ��ˮ�д�������ת��:CaO(s)+H2O(1)= Ca(OH)2(s)![]() Ca2+(aq) +2OH- (aq)����ƽ���ƶ��ĽǶȣ��������̢�NaOH������ԭ��:_______________��
Ca2+(aq) +2OH- (aq)����ƽ���ƶ��ĽǶȣ��������̢�NaOH������ԭ��:_______________��
����2:�ð�ˮ��ȥSO2
��6����֪25����NH3��H2O��Kb=1.8��10-5��H2SO3��Ka1=1.3��10-2��Ka2=6.2��10-8������ˮ��Ũ��Ϊ2.0mol/L����Һ�е�c(OH-)=________����SO2 ͨ��ð�ˮ�У���c(OH-)����1.0��10-7mol/Lʱ����Һ�е�c (SO32-)/c(HSO3-) =_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Atropic ��(H)��ijЩ�������ס���ʹ����ҩ����м��壬��һ�ֺϳ�·�����£�
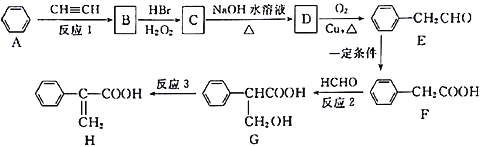
��1��G�к��������ŵ�������____________����Ӧ1Ϊ�ӳɷ�Ӧ����B�Ľṹ��ʽ��________________��
��2����Ӧ2�ķ�Ӧ����Ϊ________________����Ӧ3�ķ�Ӧ����Ϊ________________��
��3��C��D�Ļ�ѧ����ʽ��________________________________��
��4��д��E��������Һˮԡ��Ӧ�����ӷ���ʽ_______________________________��
��5������˵����ȷ����________��
a. B������ԭ�ӿ�����ͬһƽ����
b. �ϳ�·�������漰���л����Ϊ�����廯����
c.һ��������1mol�л���H�������5molH2������Ӧ
d. G�ܷ���ȡ�����ӳɡ���ȥ�����������۵ȷ�Ӧ
��6��������G�ж���ͬ���칹�壬����ͬʱ�����������������ܷ���ˮ�ⷴӦ��������Ӧ�� ������FeC13������ɫ��Ӧ���ۺ˴Ź�������ֻ��4�����շ��ͬ���칹��Ľṹ��ʽ��_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڰ����ӵ�������˵����ȷ����
A. 1mol Na2O2��Na2O�Ĺ��������У���������Ϊ3NA
B. 1mol Cl2��������NaOH��Һ��ȫ��Ӧ��ת�Ƶ��ӵ���ĿΪ2NA
C. 1mol/L��MgCl2��Һ�к��е�Cl-����ΪNA
D. 6.4gCu�ں�0.2molH2SO4��Ũ������Һ�м��ȳ�ַ�Ӧ������SO2����ķ���������Ϊ0.1NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������д������Ӽ������ۼ�����λ�����ǣ�������
A. Na2O2B. H3O+C. NH4ClD. NaOH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ϻ���һ�������Դ����,����������Щ��Դ�ǿ�ѧ�о�����Ҫ���⡣��ͼΪ��ˮ��Դ���õIJ��ֹ���,�й�˵����ȷ���ǣ� ��
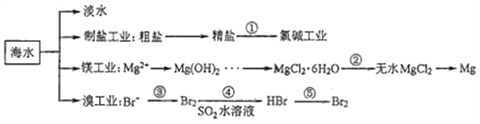
A. ��ˮ�����ķ�����Ҫ����������������������
B. �ȼҵ�в��������ӽ���Ĥ����߲�Ʒ�Ĵ���
C. ��MgCl2��6H2O�õ���ˮMgCl2�Ĺؼ���Ҫ����С����
D. �幤ҵ�Тۡ��ܵ�Ŀ����Ϊ�˸�����Ԫ�أ���Ԫ���ڷ�Ӧ�ۡ����о����������ڷ�Ӧ���б���ԭ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��E��F�Ƕ���������Ԫ��,��ԭ���������������ڶ�������AԪ��ԭ�Ӱ뾶��С��DԪ��ԭ�Ӱ뾶���B�ļ��⻯���ˮ��Һ�ʼ��ԣ�C��Eͬ����,�γɵĻ�����ΪEC2��EC3���ش���������:
��1��E��Ԫ�����ڱ��е�λ��Ϊ__________��
��2��D2E��Һ�ڿ����г��ڷ��÷�����Ӧ,������֮һΪH��H��Na2O2�Ľṹ�ͻ�ѧ�������ƣ�����Һ�Ի�ɫ��H�ĵ���ʽΪ______��
��3����ѧ�ҷ���һ�ֻ�ѧʽΪA4B4�Ļ�����ɾ���һ����ɵ�������������ɣ��������������Ϊ_______��
��4��B2A4C3��һ�ֳ�����ըҩ�����ڳ�����ײ��ʱ������һ������(B2C)��һ�ֳ���Һ�壬�÷�Ӧ�Ļ�ѧ����ʽΪ______________��8g�����ʷ�Ӧת�Ƶĵ�����ĿΪ________��
��5��������ʵ��˵��Ԫ��F�ķǽ����Ա�Ԫ��E�ķǽ�����ǿ����______��
a.Ԫ��F�γɵĵ��ʱ�Ԫ��E�γɵĵ��ʵ��۵��
b.F��E��Ԫ�صļ��⻯�����ȷֽ⣬ǰ�ߵķֽ��¶ȸ�
c.F2ͨ�뵽D2E����Һ�г��ֻ���
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com