
| A. | PbO2具有氧化性和导电性,故可作为铅蓄电池的负极材料 | |
| B. | 炭具有还原性,一定条件下能 将二氧化硅还原为硅 | |
| C. | 酒精能使蛋白质溶液沉淀析出,可以用来分离提纯蛋白质溶液 | |
| D. | Al的金属较强,可用作飞机火箭的结构材料 |
分析 A.铅蓄电池负极发生氧化反应,PbO2具有氧化性发生还原反应;
B.高温下,C能与二氧化硅反应;
C.酒精会使蛋白质发生变性;
D.铝合金的密度小、强度大,可用作飞机火箭的结构材料.
解答 解:A.铅蓄电池负极发生氧化反应,PbO2具有氧化性发生还原反应,则PbO2可作为铅蓄电池的正极材料,故A错误;
B.高温下,C能与二氧化硅反应,所以一定条件下能将二氧化硅还原为硅,故B正确;
C.酒精会使蛋白质发生变性,所以不能用酒精来分离提纯蛋白质溶液,故C错误;
D.铝合金的密度小、强度大,可用作飞机火箭的结构材料,与Al的金属性强弱无关,故D错误.
故选B.
点评 本题考查了原电池原理、C的性质、蛋白质性质、金属材料,题目涉及的知识点较多,侧重于基础知识的考查,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | Ag+、NH4+、OH-、Cl- | B. | Na+、Cu2+、SO42-、NO3- | ||
| C. | K+、Na+、SO42-、Cl- | D. | Ba2+、CO32-、NO3-、K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
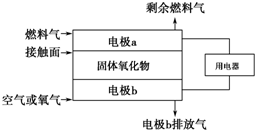 以氨作为燃料的固体氧化物(含有O2-)燃料电池,具有全固态结构、能量效率高、无污染的特点,其工作原理如图所示.下列说法正确的是( )
以氨作为燃料的固体氧化物(含有O2-)燃料电池,具有全固态结构、能量效率高、无污染的特点,其工作原理如图所示.下列说法正确的是( )| A. | 该电池工作时的总反应式为4NH3+5O2═4NO+6H2O | |
| B. | 电池工作时,接触面上的电极反应式为2NH3+3O2--6e-═N2+3H2O | |
| C. | 固体氧化物作为电池工作时的电解质,其作用是让电子在电池内部移动 | |
| D. | 外电路的电流方向为从电极a流向电极b |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将5 mL 0.02 mol/L的H2SO4溶液与5 mL 0.02 moL/L NaOH溶液充分混合,若混合后溶液的体积为10mL,則混合液的pH=2 | |
| B. | 某物质的溶液中由水电离的c(H+)=1×10-4mol/L,若a>7,則pH-定为14-a | |
| C. | pH相等的①CH3COONa ②C6H5ONa ③NaHCO3溶液中,c(Na+)大小关系:①>③>② | |
| D. | CH3COONa溶液中加入少量KNO3固体后的碱性溶液一定有:c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3-CH3和CH3-CH2-CH3 | B. | 12C和14C | ||
| C. | CH3-CH2-CH2-CH3和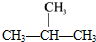 | D. | 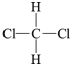 和 和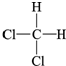 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属钠着火时,可以用二氧化碳灭火 | |
| B. | 可将金属钠存放在煤油或四氯化碳中 | |
| C. | 金属钠投入到CuSO4 溶液中,不能置换出单质铜 | |
| D. | 钠在氧气中燃烧观察到的现象是:金属钠熔化,火焰黄色,生成白色固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜和稀硝酸反应 Cu+2NO3-+4H+=Cu2++2NO2↑+2H2O | |
| B. | 锌片插入硝酸银溶液中:Zn+Ag+=Zn2++Ag | |
| C. | 氯气和氢氧化钙溶液反应 Cl2+2OH-=Cl-+ClO-+H2O | |
| D. | 盐酸和氨水反应 H++OH-=H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
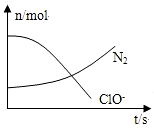
| A. | 还原剂是NH3,氧化产物是Cl- | |
| B. | 配平后氧化剂与还原剂的计量系数之比为3:2 | |
| C. | 该反应中氧化反应过程是ClO-→Cl- | |
| D. | 标准状况下,若生成2.24LN2,则转移电子为0.5 mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com