
���� ��1���¶�Խ�ߣ���Ӧ����Խ�죻
��2����������Һ��H2O2����Fe2+��Ӧ���������ӣ���ϵ���غ��ԭ���غ���ƽ��д�õ����ӷ���ʽ��
�ڸ��������Һ����ǿ�����ԣ�Ӧװ����ʽ�ζ����У�
�۸���Fe2+��KMnO4֮��Ĺ�ϵʽ���������������ʵ���������õ�Ũ�ȣ�
��Ϊʹ��Һ�е�Fe2+��ȫ��H2O2�����������������Ҫ��������ʹ��Ӧ���ַ�Ӧ��
��� �⣺��1���¶�Խ�ߣ���Ӧ����Խ�죬���Է�Ӧ���ȵ�Ŀ���Ǽӿ�����ϡ���ᷴӦ���ʣ��ʴ�Ϊ���ӿ�Fe��ϡ����ķ�Ӧ���ʣ�
��2����������Һ��H2O2����Fe2+��Ӧ���������ӣ���Ӧ�����ӷ���ʽΪ��H2O2+2Fe2++2H+=2H2O+2Fe3+��
�ʴ�Ϊ��H2O2+2Fe2++2H+=2H2O+2Fe3+��
��KMnO4����Һ����ǿ�����ԣ��������ܣ���Ҫʢ������ʽ�ζ����У�
�ʴ�Ϊ����ʽ��
�����ζ�v mL��Һ�е�Fe2+������a mol•L-1 KMnO4����Һb mL��MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O��
����Fe2+��KMnO4֮��Ĺ�ϵʽ��c��Fe2+��=$\frac{amol/L��b��1{0}^{-3}L��5}{v��1{0}^{-3}L}$=$\frac{5ab}{V}$mol/L��
�ʴ�Ϊ��$\frac{5ab}{V}$��
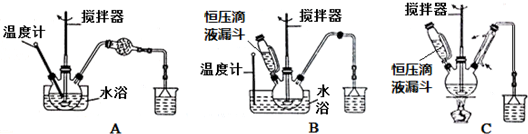
��A�������ʵ�������H2O2��Һ����������������ȫ��Ӧ����A��ȷ��
B�������μ�H2O2��Һ�����裬��Ӧ��Ӵ����������ʹ��������ȫ��Ӧ����B��ȷ��
C�����ȣ�ʹ��Ӧ�ڽϸ��¶��½��У���Ȼ��Ӧ���ʼӿ죬���ܴٽ���������ˮ����������ʣ���C����
D���ð�ˮ������ҺpH=7���������Ӻ����������ӷ�Ӧ�����������������ʣ��ʴ���
��ѡAB��
���� �����������仯����Ϊ���忼�������ʵ��Ʊ����漰������ԭ��Ӧ��ʵ���������Ӧ���ʵ�Ӱ�����ص�֪ʶ�㣬��������֮��Ĺ�ϵʽ��ʵ������Ĺ淶�ԡ�Ӱ�췴Ӧ���ʵ����ص�֪ʶ�������������Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��״���£�18g H20���Ϊ22.4L | |
| B�� | 2L 0.5mol/L CH3COOH��Һ�к��е�H+����ĿΪNA | |
| C�� | 0.1molп������ϡ���ᷴӦ��ת�Ƶĵ�����Ϊ0.1NA | |
| D�� | ���³�ѹ��4.6g NO2��N2O4�Ļ�����壬ԭ����Ϊ0.3NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| HA | H2B | H2C | H3D |
| 1.8��10-5 | K1=4.3��10-7 K2=5.6��10-11 | K1=9.1��10-8 K2=1.1��10-12 | K1=7.5��10-3 K2=6.2��10-8 K3=2.2��10-13 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ����ʡ��2013��12��1����ʱ�𣬳�����������Ϊ�������������Զ���������ŷ����˴��ĸ��ƣ���֪SO2������Fe�� NO3��3��Һ���գ�0.1mol/L��Fe��NO3��3��Һ��pH=2ijѧϰС��ݴ�չ���������̽����
����ʡ��2013��12��1����ʱ�𣬳�����������Ϊ�������������Զ���������ŷ����˴��ĸ��ƣ���֪SO2������Fe�� NO3��3��Һ���գ�0.1mol/L��Fe��NO3��3��Һ��pH=2ijѧϰС��ݴ�չ���������̽�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �������� | ��������� | �������� | �廯�� | �Ȼ��� |
| ˮ�е��ܽ��� | ��������ˮ��������ˮ | ���� | ���� | ���� |
| �Ҵ��е��ܽ��� | �� | �� | ���� | ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ǿ | B�� | ���� | C�� | ���� | D�� | ���ж� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 $\stackrel{��������}{��}$
$\stackrel{��������}{��}$ ��R��R�����������
��R��R����������� ��
�� ��
���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com