
【题目】X、Y、Z、Q、R是五种短周期元素,原了序数依次增大。X、Y两元素最高正价与最低负价之和均为0;Q与X同主族;Z、R分别是地壳中含量最高的非金属元素和金属元素。请回答下列问题:
(1)五种元素原子半径由大到小的顺序是(写元素符号)______________。
(2)X与Z能形成多种化合物,其中相对分了质量是34的分子的结构式为___________。
(3)由以上某些元素组成的化合物A、B、C、D有如下转化关系:![]() (在水溶液中进行)。其中,C是溶于水显酸性的气体;D是淡黄色固体。写出D的电子式_______。
(在水溶液中进行)。其中,C是溶于水显酸性的气体;D是淡黄色固体。写出D的电子式_______。
①如果A、B均由三种元素组成,B为两性不溶物,由A转化为B的离子方程式为______。
②如果A由三种元素组成,B由四种元素组成,A、B溶液均显碱性,由A转化为B的离子方程式为_________________。
【答案】 Na>Cl>C>O>H H-O-O-H ![]() CO2+AlO2-+2H2O=Al(OH)3↓+HCO3-(或CO2+2AlO2-+3H2O=2Al(OH)3↓+CO32-) CO2+H2O+CO32-=2HCO3-
CO2+AlO2-+2H2O=Al(OH)3↓+HCO3-(或CO2+2AlO2-+3H2O=2Al(OH)3↓+CO32-) CO2+H2O+CO32-=2HCO3-
【解析】X、Y、Z、Q、R是五种短周期元素,原子序数依次增大,Z、R分别是地壳中含量最高的非金属元素和金属元素,则Z为O元素、R为Al;X、Y两元素最高正价与最低负价代数和均为0,原子序数均小于O元素,为ⅠA族元素、ⅣA族元素,故X为H元素、Y为C元素;Q与X同主族,结合原子序数可知,Q为Na元素,据此分析解答。
根据以上分析可知X、Y、Z、Q、R分别是H、C、O、Na、Al。则
(1)同周期自左而右,原子半径逐渐减小,电子层越多,原子半径越大,故原子半径由大到小的顺序是:Na>Al>C>O>H;
(2)O和H能形成多种化合物,其中相对分子质量是34的分子为双氧水,含有氢氧单键和氧氧单键,结构式为H-O-O-H;
(3)由以上某些元素组成的化合物A、B、C、D有如下转化关系:![]() (在水溶液中进行),其中C是溶于水显酸性的气体,D是淡黄色固体,则D是Na2O2,C是CO2,过氧化钠是离子化合物,电子式为
(在水溶液中进行),其中C是溶于水显酸性的气体,D是淡黄色固体,则D是Na2O2,C是CO2,过氧化钠是离子化合物,电子式为![]() ;
;
①如果A、B均由三种元素组成,B为两性不溶物,则B是Al(OH)3,D是过氧化钠、C是二氧化碳,A是偏铝酸钠,偏铝酸钠和二氧化碳反应生成氢氧化铝和碳酸根离子或碳酸氢根离子,离子反应方程式为:AlO2-+2H2O+CO2=Al(OH)3+HCO3-或2AlO2-+3H2O+CO2=2Al(OH)3+CO32-;
②如果A由三种元素组成,B由四种元素组成,A、B溶液均显碱性,则A为Na2CO3、B为NaHCO3,碳酸钠转化为碳酸氢钠的离子方程式为CO32-+H2O+CO2=2HCO3-。


 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案科目:高中化学 来源: 题型:
【题目】某新型电池,以NaBH4(B的化合价为+3价)和H2O2作原料,负极材料采用Pt,正极材料采用MnO2(既作电极材料又对该极的电极反应具有催化作用),该电池可用作卫星、深水勘探等无空气环境电源,其工作原理如图所示。下列说法不正确的是

A. 每消耗3mol H2O2,转移6mol e﹣
B. 电池工作时Na+从b极区移向a极区
C. a极上的电极反应式为:BH4﹣+8OH﹣﹣8e﹣═BO2﹣+6H2O
D. b极材料是MnO2,该电池总反应方程式:NaBH4 + 4H2O2===NaBO2 + 6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业焊接钢管常用55137Cs进行“无损探伤”.下列有关说法正确的是( )
A.137表示质量数
B.137表示质子数
C.该原子质子数大于中子数
D.55表示中子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,对于可逆反应X(g)+3Y(g)![]() 2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.08 mol·L-1,则下列判断正确的是( )
2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.08 mol·L-1,则下列判断正确的是( )
A. c1∶c2=3∶1 B. 平衡时,Y和Z的生成速率之比为2∶3
C. X、Y的转化率不相等 D. c1的取值范围为0<c1<0.14 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示不同温度下水溶液中c(H+)与c(OH﹣)的关系,下列判断正确的是( )
A.两条曲线上任意点均有c(H+)×c (OH﹣)=Kw
B.T<25
C.b点和c点pH均为6,溶液呈酸性
D.只采用升温的方式,可由a点变成d点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)为了验证Fe3+与Cu2+氧化性强弱,下列装置能达到实验目的的是_______。

(2)将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。
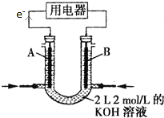
A处其电极反应式为___________;
(3)某元素的同位素![]() ,它的氯化物XCl21.11g溶于水配成溶液后,加入1mo1/L的AgNO3溶液20mL,恰好完全反应。若这种同位素的原子核内有20个中子,Z的值为_____,A的值为______。
,它的氯化物XCl21.11g溶于水配成溶液后,加入1mo1/L的AgNO3溶液20mL,恰好完全反应。若这种同位素的原子核内有20个中子,Z的值为_____,A的值为______。
(4)将固体NH4Br置于密闭容器中,在某温度下,发生下列反应:
NH4Br(s)![]() NH3(g)+HBr(g) 2HBr(g)
NH3(g)+HBr(g) 2HBr(g)![]() Br2(g)+H2(g)
Br2(g)+H2(g)
2min后,测知c(H2)=0.5mo/L,c(HBr)=4mol/L。若上述反应速率用v(NH3)表示,则v(NH3)=_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的数值,下列说法不正确的是
A. 1mol甲基(-CH3)中含有的电子数为9NA
B. 标准状况下,22.4LCH2=CH2中含C-H数为4NA
C. 1mol分子式为C2H6O的物质,含O-H数一定是NA
D. 0.1mol由乙烯与乙醇组成的混合物完全燃烧所消托的氧气分子数为0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某公司设计的用于驱动潜艇的液氨﹣液氧燃料电池示意图如下,有关说法正确的是( )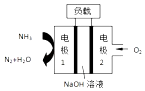
A.电池总反应为:4NH3+3O2=2N2+6H2O
B.电池工作时,OH﹣向正极移动
C.电极 2 发生的电极反应为:O2+4H++4e﹣=2H2O
D.电流由电极 1 经外电路流向电极2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com