
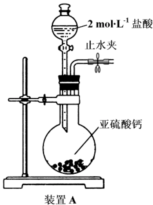


分析 (1)盐酸与亚硫酸钙反应生成氯化钙、二氧化硫与水;
(2)二氧化硫与氢硫酸反应生成硫,反应中二氧化硫表现氧化性;
(3)次氯酸具有强氧化性、二氧化硫具有还原性,不能利用二氧化硫与次氯酸钙直接反应判断亚硫酸与次氯酸的酸性强弱,先验证亚硫酸酸性比碳酸强,再结合碳酸酸性比HClO强碱性判断.A装置制备二氧化硫,由于盐酸易挥发,制备的二氧化硫中混有HCl,用饱和的亚硫酸氢钠除去HCl,再通过碳酸氢钠溶液,可以验证亚硫酸酸性比碳酸强,用酸性高锰酸钾溶液氧化除去二氧化碳中的二氧化硫,用品红溶液检验二氧化碳中二氧化硫是否除尽,再通入F中;
(4)①采取逆流原理通入冷凝水;
②根据关系式:SO2~H2SO4~2NaOH计算;
③残留液中有剩余的盐酸.
解答 解:(1)盐酸与亚硫酸钙反应生成氯化钙、二氧化硫与水,反应方程式为:CaSO3+2HCl=CaCl2+SO2↑+H2O,
故答案为:CaSO3+2HCl=CaCl2+SO2↑+H2O;
(2)二氧化硫与氢硫酸反应生成硫,反应中二氧化硫表现氧化性,利用装置1中产生的气体证明+4价硫具有氧化性:将SO2通入氢硫酸溶液中,出现淡黄色沉淀,证明+4价硫具有氧化性,
故答案为:将SO2通入氢硫酸溶液溶液中,出现淡黄色沉淀,证明+4价硫具有氧化性;
(3)次氯酸具有强氧化性、二氧化硫具有还原性,不能利用二氧化硫与次氯酸钙直接反应判断亚硫酸与次氯酸的酸性强弱,先验证亚硫酸酸性比碳酸强,再结合碳酸酸性比HClO强碱性判断.A装置制备二氧化硫,由于盐酸易挥发,制备的二氧化硫中混有HCl,用饱和的亚硫酸氢钠除去HCl,再通过碳酸氢钠溶液,可以验证亚硫酸酸性比碳酸强,用酸性高锰酸钾溶液氧化除去二氧化碳中的二氧化硫,用品红溶液检验二氧化碳中二氧化硫是否除尽,再通入F中,则:
装置连接顺序为A、C、B、E、D、F,其中装置C的作用是除去HCl气体,D中品红不褪色,F中出现白色沉淀,可证明亚硫酸的酸性强于次氯酸,
故答案为:B、E;除去HCl;D中品红不褪色,F中出现白色沉淀;
(4)①采取逆流原理通入冷凝水,即球形冷凝管进水口为b,故答案为:b;
②设残液中SO2含量为xg.L-1,则:
SO2~~H2SO4~~2NaOH
64g 2mol
xg.L-1×0.001L 0.02L×0.1mol/L
所以64g:xg.L-1×0.001L=2mol:0.02L×0.1mol/L
解得x=64.00
故答案为:64.00;
③残留液中有剩余的盐酸,挥发出HCl,会消耗NaOH,导致测定值始终高于实际值,
故答案为:残留液中有剩余的盐酸.
点评 本题考查气体制备与性质实验、物质含量测定实验,涉及装置分析与评价、实验方案设计、仪器使用、化学计算等,关键是明确实验原理,较好的考查学生实验综合能力与知识迁移应用,难度中等.


科目:高中化学 来源: 题型:解答题
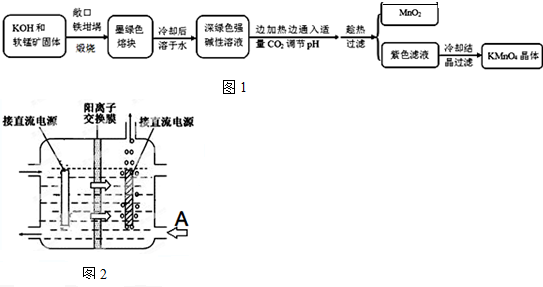
| 物质 | KMnO4 | K2CO3 | KHCO3 | K2SO4 | CH3COOK |
| 20℃溶解度 | 6.4 | 111 | 33.7 | 11.1 | 217 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
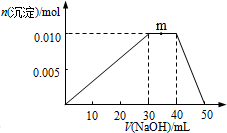
| A. | NH4Al(SO4)2的电离方程式为:NH4Al(SO4)2?NH4++Al3++2SO42- | |
| B. | m点反应的离子方程式:NH4++OH-═NH3•H2O | |
| C. | 反应过程中SO42-的浓度始终保持不变 | |
| D. | 由图象可知所滴NaOH溶液的浓度为0.1mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
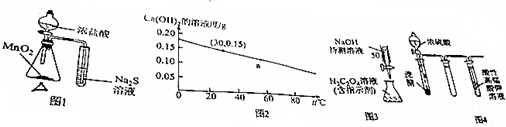
| A. | 图1的装置可用于比较MnO2、Cl2、S的氧化性 | |
| B. | 图2可知:30℃时Ca(OH)2溶液的浓度一定大于60℃时的温度 | |
| C. | 图3的装置可用于已知浓度的H2C2O4溶液测定未知浓度的NaOH溶液 | |
| D. | 图4的实验现象:酸性高锰酸钾溶液中有气泡出现,且溶液颜色逐渐变浅乃至褪去 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
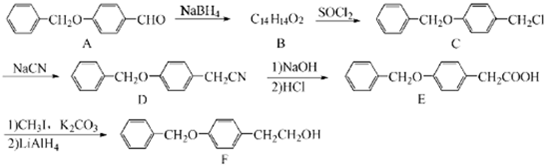
 ;由C→D的反应类型是:取代反应.
;由C→D的反应类型是:取代反应.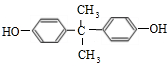
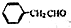 为原料制备
为原料制备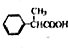 的合成路线示意图(无机试剂任用).合成路线示意图例如题干.
的合成路线示意图(无机试剂任用).合成路线示意图例如题干.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 80 | 100 |
| Li2CO3 | 1.54 | 1.43 | 1.33 | 1.25 | 1.17 | 1.08 | 1.01 | 0.85 | 0.72 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

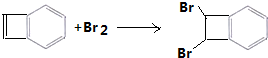
 +2CH3CH2OH$?_{△}^{浓硫酸}$
+2CH3CH2OH$?_{△}^{浓硫酸}$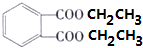 +2H2O
+2H2O查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 平衡向正反应方向移动 | B. | a+b>c+d | ||
| C. | C的体积分数降低 | D. | B的转化率升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钢铁腐蚀的负极反应为:Fe-3e-=Fe3+ | |
| B. | Mg-Al及NaOH溶液构成的原电池中负极材料为Mg | |
| C. | 无隔膜电解饱和NaCl溶液所得产物之一是“84”消毒液中的有效成分NaClO | |
| D. | H2-O2燃料电池中电解液为H2SO4,则正极反应式为:O2+4e-=2O2- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com