
某研究性学习小组设计了一组实验验证元素周期律。
(1)甲同学在a、b、c三只烧杯里分别加入50 mL水,再分别滴加几滴酚酞溶液,依次加入大小相近的锂、钠、钾块,观察现象。
①甲同学设计实验的目的是________________________________________________;
②反应最剧烈的烧杯是_______(填字母);
③写出b烧杯里发生反应的离子方程式______ _____ __。
(2)乙同学设计实验验证非金属元素的非金属性越强,对应的最高价含氧酸的酸性就越强。他设计了下图装置以验证碳、氮、硅元素的非金属性强弱。
乙同学设计的实验可直接证明三种酸的酸性强弱,已知A是强酸,常温下可与铜反应;B是块状固体;打开分液漏斗的活塞后,C中可观察到白色沉淀生成。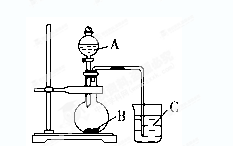
①写出所选用物质的化学式:A、________; B、________;C、________。
②写出烧瓶中发生反应的化学方程式:
___________________________________________________________。
③写出烧杯中发生反应的化学方程式:
___________________________________________________________。
④碳、氮、硅元素的非金属性强弱顺序为_______________________。
(Ⅰ) ①验证锂、钠、钾的活泼性(或同一主族,从上到下元素的金属性逐渐增强)(2分)
②c(2分)
③2 Na+2H2O=2Na++2OH—+H2↑(2分)
(Ⅱ) ①CaCO3 (1分)Na2SiO3(或K2SiO3) (1分)
②2HNO3+CaCO3=Ca(NO3) 2+H2O+CO2↑(2分)
③CO2+H2O+Na2SiO3 =H2SiO3↓+Na2CO3(2分)
或2CO2+2H2O+Na2SiO3=H2SiO3↓+2NaHCO3
④氮>碳>硅(1分)
解析试题分析:钠与钾都属于碱金属元素位于第一主族。其最外层都为一个电子,都易失去电子表现出较强的还原性。其化学性质相似。本实验主要验证钠与钾的活泼性强弱的比较。据题意可知A为硝酸。B为碳酸钙。C为硅酸钠、硝酸与碳酸钙反应生成二氧化碳逸出到烧杯C中,烧杯中出现白色沉淀,这个白色沉淀应该是硅酸。硅酸是一种不溶于水的酸。所以非金属线由强到弱的顺序为;氮、碳、硅。
考点:考查验证元素性质的相关知识


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:填空题
现有四种短周期元素X、Y、Z、W,其中:
① X、W原子的电子层数与最外层电子数之比分别为3:1和1:3
② Y原子是元素周期表中原子半径最小的
③ Z是形成化合物种类最多的元素
回答下列问题:
(1)X元素在周期表中的位置是 。
(2)上述四种元素中所能组成的含有非极性共价键的化合物的分子式 (填其中一种即可)。
(3)化合物X2W2的电子式是 。
(4)向含1 mol Na2SiO3的溶液中缓慢通入2 mol的ZO2,反应的离子方程式是 。
(5)由Y、Z、W元素中的两种或三种可以组成多种分子,其中含有10个电子的分子是_________(填化学式)。
(6)向25.00 mL的Y2Z2W4溶液中加入5.00 mL 0.50 mol/L酸性KMnO4溶液恰好完全反应,得到ZO2和Mn2+,则此种Y2Z2W4溶液的物质的量浓度是 mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:问答题
(12分)A、B、C、D、E、F六种元素分属三个短周期,且原子序数依次增大。A、D同主族,可形成离子化合物X;B的氢化物与F的氢化物可反应生成离子化合物Y, 且B的单质是空气中含量最高的物质;C原子的最外层电子是次外层电子数的3倍;D、E、F 3种原子最外层共有11个电子, 且这3种元素的最高价氧化物的水化物两两皆能发生反应生成盐和水。
(1)B元素的名称是________,B单质的结构式为_____________。
(2)用电子式表示化合物X的形成过程__________________________________。
(3)化合物Y的电子式为_____________,A2C2的电子式为_____________。
(4)D、E最高价氧化物的水化物之间反应的离子方程式为 ___________。
查看答案和解析>>
科目:高中化学 来源: 题型:问答题
今有甲、乙、丙、丁四种元素。已知:甲元素是自然界中含量最多的元素;乙元素为金属元素,它的原子核外K层、L层电子数之和等于M、N层电子数之和;丙元素的单质及其化合物的焰色反应都显黄色;氢气在丁元素单质中燃烧火焰呈苍白色。
(1)试推断并写出甲、乙、丙、丁四种元素的名称和符号;
(2)写出几种上述元素两两化合形成的化合物的化学式。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某同学想探究硫和碳原子的得电子能力的强弱,通过比较它们最高价氧化物对应水化物的酸性强弱来验证,设计了如图实验,请回答: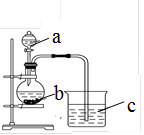
(1)仪器a的名称是 ,应盛放下列药品中的 (填序号)。
A.稀硫酸 B. 亚硫酸 C. 氢硫酸 D. 盐酸
(2)仪器b应盛放下列药品中的 (填序号)。
A.碳酸钙 B. 硫酸钠 C. 氯化钠 D. 碳酸钠
(3)b中反应的离子方程式为 。
若看到仪器C中的现象是 ,即可证明 比 酸性强(填化学式),得电子的能力 比 强。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关叙述中,不可以用氢键来解释的是
| A.0℃时,水的密度大于冰的密度 | B.水的熔沸点高于硫化氢的熔沸点 |
| C.氟化氢气体极易溶于水 | D.氟化氢比氯化氢稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
用价电子对互斥理论(VSEPR)可以预测许多分子或离子的空间构型,也可推测键角大小,下列判断正确的是
| A.CS2是V形分子 | B.SnBr2键角大于120° |
| C.BF3是三角锥形分子 | D.NH4+键角等于109.5° |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com