
��10�֣�ijͬѧ�ù�ҵ����ͭ�����������������ʣ��Ʊ�������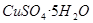 ��
��
I.ȡ��ҵ����ͭ���壬��ϡ�����ܽ⣬���ˡ�
II.����Һ�еμ�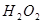 ��Һ���Լ��ȡ�
��Һ���Լ��ȡ�
III.��II����Һ�м���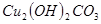 ��ĩ��
��ĩ��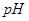 Ϊ
Ϊ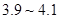 ��
��
IV.������У����ˣ���Һ��ϡ�����ữ�� ��
��
V. ����Ũ������ȴ�ᾧ�����ˣ��þ��塣
��֪�����������������������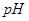 ���±���
���±���
| ���� | 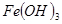 | 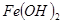 | 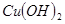 |
��ʼ����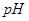 | 2.7 | 7.6 | 4.7 |
��ȫ����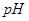 | 3.7 | 9.6 | 6.7 |
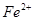 ����Ϊ
����Ϊ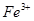 ��Ŀ���� ��
��Ŀ���� ��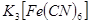 �����軯�أ���֤II��
�����軯�أ���֤II��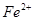 �Ƿ�ת����ȫ�������� ��
�Ƿ�ת����ȫ�������� ����10�֣���ÿ��2�֣� ��1��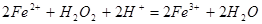
��2����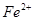 ����Ϊ
����Ϊ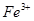 �������ڵ���
�������ڵ���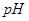 Ϊ3.9~4.1ʱ��ֻ��
Ϊ3.9~4.1ʱ��ֻ��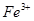 ת��Ϊ������ȥ��������ʹ
ת��Ϊ������ȥ��������ʹ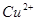 ת��Ϊ�������������������ɵ÷֣�
ת��Ϊ�������������������ɵ÷֣�
��3��������ɫ������˵��˵��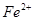 û����ȫת������û����ɫ�������ɣ�˵��
û����ȫת������û����ɫ�������ɣ�˵��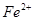 �Ѿ���ȫת������ֻ�������һ�������������ȷ�����֡���
�Ѿ���ȫת������ֻ�������һ�������������ȷ�����֡���
��4�� ����д��ȷ���ɵõ�2�֣�
����д��ȷ���ɵõ�2�֣�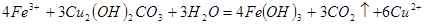 ����д���۷֣�
����д���۷֣�
��5����ϡ�����ữ�� ����������
����������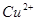 �ڼ��ȹ�����ˮ�⣬�Ի�ô���������ͭ���塣�������������ɵ÷֣�
�ڼ��ȹ�����ˮ�⣬�Ի�ô���������ͭ���塣�������������ɵ÷֣�
����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| �� |
| �� |
| �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����

| ���� | Cu��OH��2 | Fe��OH��2 | Fe��OH��3 |
| ��ʼ����pH | 6.0 | 7.5 | 1.4 |
| ������ȫpH | 13 | 14 | 3.7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ���� | Fe��OH��3 | Fe��OH��2 | Cu��OH��2 |
| ��ʼ����pH | 2.7 | 7.6 | 4.7 |
| ��ȫ����pH | 3.7 | 9.6 | 6.7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
(1)�Ʊ�����ͭ
![]() CuSO4��5H2O����CuO
CuSO4��5H2O����CuO
�ٲ�����Ŀ���dz����������ʡ�������___________________________________________��
�ڲ�����Ŀ���dz����������ǣ��μ�H2O2��Һ���Լ��ȣ�Fe2+ת����ȫ����������Cu2(OH)2CO3��ĩ�����裬�Կ�����ҺpH=3.5���������һ��ʱ�䣬���ˣ���ϡ�����ữ��Һ��pH=1��������ҺpH=3.5��ԭ����_________��
�۲�����Ŀ���ǵõ�CuSO4��5H2O���壬������__________________��ˮԡ���Ⱥ�ɡ�ˮԡ���ȵ��ص���___________________________________________________________��
(2)̽������ͭ����
��ȡA��B��֧�Թܣ���A���ȼ�������CuO��ĩ���ٷֱ���A��B�м���������3%H2O2��Һ��ֻ�۲쵽A���д������ݣ�������____________________________________________��
��Ϊ̽���Թ�A�з�Ӧ�����ʣ��ռ����岢�ⶨ����������ʵ��������______________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com