
| X | ||||
| W | Y | Z |
| A、元素Z位于元素周期表的第3周期ⅦA族 |
| B、原子半径的大小顺序为:rY>rW>rX |
| C、元素W的最高价氧化物对应水化物的酸性比Y的强 |
| D、元素X的气态简单氢化物的热稳定性比W的强 |


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:
| A、用石灰石中和酸性土壤 |
| B、用盐酸除铁锈 |
| C、用FeCl3溶液刻制铜材电路板 |
| D、铝锅表面生成致密的薄膜 |
查看答案和解析>>
科目:高中化学 来源: 题型:
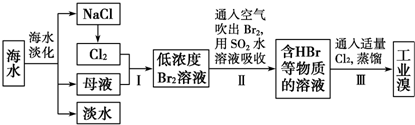
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X、M两种元素只能形成X2M型化合物 |
| B、由于W、Z、M元素的氢化物的相对分子质量依次减小,所以其沸点依次降低 |
| C、元素X、Z、W的单质晶体中含相同类型的化学键 |
| D、元素W和M的某些单质可作为水处理中的消毒剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com