
分析 (1)放电时,铅蓄电池的负极发生氧化反应,而铅离子与溶液中的硫酸根离子生成难溶的硫酸铅,电极反应式为:Pb-2e-+SO42-=PbSO4;
(2)原电池工作时电子由负极流向正极;
(3)铅蓄电池中铅是负极,207g铅消耗时转移 2mol e-,故钠硫电池的理论放电量是铅蓄电池的$\frac{207}{46}$=4.5 倍;
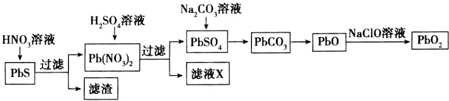
Ⅱ.(1)①过氧化氢将黑色PbS氧化成白色的硫酸铅,所以过氧化氢是氧化剂;
②已知硫化铅溶于水时存在溶解平衡:PbS(s)?Pb2+(aq)+S2-(aq),电离产生的硫离子具有还原性,而硝酸具有强氧化性,发生氧化还原反应,导致硫离子的浓度减少,固平衡正向移动;
(2)硝酸铅与硫酸发生复分解反应生成难溶硫酸铅,和硝酸;残留的SO42-过多,会与溶液中的铅离子结合成难溶的硫酸铅,导致铅的流失,减少了二氧化铅的产量;
(3)①PbO和次氯酸钠反应生成二氧化铅和氯化钠;②电解时,阳极上铅离子失电子和水反应生成二氧化铅;加入硫酸铜,铜离子在阴极放电生成单质铜,避免了铅离子放电,从而大大提高铅离子的利用率.
解答 解:(1)放电时,铅蓄电池的负极发生氧化反应,而铅离子与溶液中的硫酸根离子生成难溶的硫酸铅,电极反应式为:Pb-2e-+SO42-=PbSO4,故答案为:Pb-2e-+SO42-=PbSO4;
(2)原电池工作时电子由负极流向正极,故答案为:正极;
(3)铅蓄电池中铅是负极,207g铅消耗时转移 2mol e-,故钠硫电池的理论放电量是铅蓄电池的:$\frac{207}{46}$=4.5 倍,故答案为:4.5;
Ⅱ.(1)①过氧化氢将黑色PbS氧化成白色的硫酸铅,所以过氧化氢是氧化剂,故答案为:氧化剂;
②已知硫化铅溶于水时存在溶解平衡:PbS(s)?Pb2+(aq)+S2-(aq),电离产生的硫离子具有还原性,而硝酸具有强氧化性,发生氧化还原反应,导致硫离子的浓度减少,固平衡正向移动,故答案为:硝酸氧化硫离子导致硫离子的浓度减小,使溶解平衡正向移动,促进PbS的溶解;
(2)硝酸铅与硫酸发生复分解反应生成难溶硫酸铅,和硝酸;残留的SO42-过多,会与溶液中的铅离子结合成难溶的硫酸铅,导致铅的流失,减少了二氧化铅的产量,故答案为:HNO3;浸出时部分铅离子生成硫酸铅随浸出渣排出,降低硫酸铅的产率;
(3)①PbO和次氯酸钠反应生成二氧化铅和氯化钠,离子方程式为PbO+ClO-=PbO2+Cl-;②电解时,阳极上铅离子失电子和水反应生成二氧化铅,电极反应式为Pb2++2H2O-2e-=PbO2↓+4H+;加入硫酸铜,铜离子在阴极放电生成单质铜,避免了铅离子放电,从而大大提高铅离子的利用率,
故答案为:PbO+ClO-=PbO2+Cl-;Pb2++2H2O-2e-=PbO2↓+4H+,加入硫酸铜,铜离子在阴极放电生成单质铜,避免了铅离子在阴极放电,增大铅离子的利用率.
点评 本题考查电化学的相关知识,涉及物质的量的有关计算、离子反应、电解原理等知识点,注意(3)中阳极、阴极电极反应式的书写,为易错点.


科目:高中化学 来源: 题型:选择题
| B | C |
| D |
| A. | 简单离子的半径大小关系:B>C>E | |
| B. | D、E两种元素形成的化合物,可能含有离子键和共价键 | |
| C. | A、B、C三种元素形成的化合物,晶体类型一定相同 | |
| D. | B、D分别和C形成的化合物,都有可能使溴水或品红溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
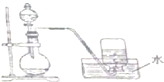
| A. | 氯酸钾和二氧化锰的混合物制取氧气 | |
| B. | 石灰石和盐酸制取二氧化碳 | |
| C. | 浓盐酸和二氧化锰制取氯气 | |
| D. | 铜与稀硝酸反应制取一氧化氮 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 标况下11.2L乙烷分子中所含分子数为0.5NA | |
| B. | 1.8g的NH4+中含有的电子数为0.1NA | |
| C. | 20克氖气所含原子数为0.5NA | |
| D. | 常温常压下,48g O3和O2的混合气体中,含有氧原子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在硫酸铜溶液中加入过量氢氧化钡溶液 Ba2++SO42-=BaSO4↓ | |
| B. | 钠与水的反应Na+2H2O═Na++2OH-+H2↑ | |
| C. | 氯气通入氢氧化钠溶液中 2Cl2+2OH-=3Cl-+ClO-+H2O | |
| D. | 大理石溶于醋酸的反应CaCO3+2CH3COOH═Ca2++2CH3COO-+CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 用途 | 解释 |
| A | 硅胶可作袋装食品的干燥剂 | 硅胶多孔,吸收空气中氧气的能力强 |
| B | CuSO4可作游泳池的消毒剂 | 铜盐能使构成病毒的蛋白质变性 |
| C | 浸有高锰酸钾溶液的硅藻土可作某些水果的保鲜剂 | 高锰酸钾溶液能氧化水果释放的催熟剂乙烯 |
| D | Na2O2可作呼吸面具中的供氧剂 | Na2O2能吸收CO2同时放出O2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com