
I. 下面列出了几组物质或粒子,请将合适的组号填写在空格上。
①金刚石与“足球烯”(C60)
②CH3CH2CH2CH(C2H5)CH3 和 CH3CH2CH2CH(CH3)C2H5
③235U、238U ④氧气(O2)与臭氧(O3)
⑤乙醇(CH3CH2OH)和甲醚(CH3OCH3) ⑥淀粉和纤维素
⑦ 
(1)是同素异形体的是 ,(填序号,下同)
(2)是同位素的是 ,
(3)是同分异构体的是 ,
(4)是同一物质的是 。
II. 下列物质:①Cl2 ②Na2O2 ③NaOH ④HCl ⑤C2H6 ⑥MgF2 ⑦HNO3
(1)只由离子键构成的物质是______________(填序号,下同)(2)由离子键和非极性键构成的物质是______________(3)由极性键和非极性键构成的物质是______________
III. 提纯下列物质(括号内的物质是杂质),请将所选用的除杂试剂和分离方法(填字母或者序号)填入对应的空格中(若不选,填“无”)
除杂试剂:A. 盐酸 B. 酸性高锰酸钾 C. 氢氧化钠溶液 D. (浓)溴水
E. H2(催化剂) F. CaO G. NaCl
分离方法:① 蒸馏 ② 分液 ③ 洗气 ④ 过滤
| 被提纯的物质 | 除杂试剂 | 分离方法 | |
| (1) | 酒精(水) | ||
| (2) | 乙烷(乙烯) | ||
| (3) | 硬脂酸钠溶液(甘油) | ||
| (4) | 苯(苯酚) | ||
| (5) | SiO2(Al2O3) |
【知识点】化学用语,物质的结构,物质的除杂 A4 E3 J2
【答案解析】I. (1)①④ (2) ③ (3) ⑤ (4)②⑦
II. (1)⑥ (2)② (3)⑤
III.
| 被提纯的物质 | 除杂试剂 | 分离方法 | |
| (1) | 酒精(水) | F | ① |
| (2) | 乙烷(乙烯) | D | ③ |
| (3) | 硬脂酸钠溶液(甘油) | G | ④ |
| (4) | 苯(苯酚) | C | ② |
| (5) | SiO2(Al2O3) | A | ④ |
解析:I、同素异形体是同一种元素形成的不同种物质,故有①④;同位素是质子数相同、中子数不同的同一元素形成的不同原子,故为③;同分异构体是相同的分子式、不同的结构的有机物之间的关系,故为⑤;是同一物质的是②⑦。
II.在⑥MgF2在只存在着离子键;在②Na2O2既由离子键又有共价键;在⑤C2H6中既由极性键和非极性键。
III. (1) 酒精中的水选用CaO和水发生反应然后进行蒸馏的方法;(2) 乙烷中的乙烯除杂的方法可以让混合气体通过溴水,乙烯和溴发生加成反应生成1,2—二溴乙烷存在在溶液中而除去乙烯;(3) NaCl可以降低甘油在硬脂酸钠溶液的溶解度而除去;(4)苯酚可以与碱液发生反应生成易溶于水的物质,而苯是难溶于水的,在利用分液的方法除去;(5) Al2O3是两性物质,而SiO2是酸性氧化物,故可以采用盐酸进行除杂。
【思路点拨】本题考查了化学基本用语、物质的结构、物质的除杂,涉及的知识点比较多,基础性较强。


科目:高中化学 来源: 题型:
查文献知,CH3COOH、H3PO3(二元酸)、H3PO4三种酸所有的逐级电离常数如下:
| 酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) |
| CH3COOH | 1.8×10-5 | H3PO4 | K1=7.1×10-3 |
| H3PO3 | K1=3.7×10-2 | K2=6.2×10-8 | |
| K2 =2.9×10-7 | K3=4.5×10-13 |
用化学用语回答下列问题:
(1)上述三种酸中,酸性最强的是 ;
(2)常温下,在NaH2PO3稀溶液中:c(H3PO3) < c(HPO32-),则该溶液pH_______7;(填“>”“<”或“=”)
(3)等温度、等浓度的NaH2PO4溶液与Na2HPO4溶液比较,c(H3PO4)较大的是:___ __;
(4)25℃时,浓度均为0.01 mol/L 的CH3COONa、Na2HPO3、Na3PO4溶液,pH最大的是:_________________;
(5)在NaH2PO3溶液中,粒子间存在等量关系:c(H3PO3)+_____________= c(Na+)。(用溶液中其它粒子浓度补充完整)
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室中需要配制2 mol/L的NaCl溶液950 mL,配制时应选用的容量瓶的规格和称取的NaCl的质量分别是 ( )
A.950 mL 111.2 g B.500 mL 117.0 g
C.任意规格 111.2 g D.1000 mL  117.0 g
117.0 g
查看答案和解析>>
科目:高中化学 来源: 题型:
某氯化镁溶液的密度为1.18 g·cm-3,其中镁离子的质量分数为5.1%,300 mL该溶液中Cl-的物质的量约等于( )
A.0.37 mol B. 0.63 mol C.0.74 mol D.1.5 mol
0.63 mol C.0.74 mol D.1.5 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
NA为阿伏伽德罗常数,下列叙述错误的是
A.常温常压下,42g乙烯和丁烯混合气体中,极性键数为 6 NA
B.1 mol Mg与足量O2或N2反应生成MgO或Mg3N2均失去2 NA个电子
C.由CO2和O2组成的混合气体中共有NA个分子,其中的氧原子数为2NA
D.6.4g SO2与足量氧气反应生成SO3,转移电子数为0.2 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质分类正确的是 ( )
A.Cu(OH)2难溶于水,属于非电解质
B.SO2能与碱反应生成盐和水,属于酸性氧化物
C.NH4Cl组成中不含金属离子,不属于盐
D.HCl气体溶于水电离成H+和Cl-,属于离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
我国科学家为一个比头发丝还细的小分子恢复了磁性,由此创造了一项“世界第一”。实验时将一种名为“钴酞菁”的小分子搬上了“手术台”。这个“个头”仅为1.3纳米的小分子,其结构和性质与人体内的血红素及植物体内的叶绿素非常相似,在光电子器件、生物技术等方面具有广泛而重要的应用与研究价值。下列说法正确的是( )
A.“钴酞菁”的小分子没有胶体粒子的性质;
B.纳米材料可以应用于所有化工领域;
C.现在纳米器件都是无所不能的胶体
D.此工作实现了利用局域的化学反应来改变和控制分子的物理性质
查看答案和解析>>
科目:高中化学 来源: 题型:
合成氨工业对国民经济和社会发展具有重要的意义.对于密闭容器中的反应:N2(g)+3H2(g) 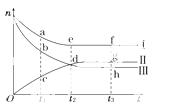
 2NH3(g),500 K、30 MPa下n(NH3)、n(H2)和n(N2)随时间变化的关系如图所示
2NH3(g),500 K、30 MPa下n(NH3)、n(H2)和n(N2)随时间变化的关系如图所示
请回答下列问题:
(1)上图中属于氢气物质的量随时间变化的曲线是______(填“Ⅰ”、“Ⅱ”或 “Ⅲ”).
(2)关于t2时刻的说法正确的是________.
A.t2时该反应达到平衡状态
B.t2时Ⅱ和Ⅲ代表的物质反应速率相同
C.t2时氢气、氮气与氨气的反应速率之比为3∶1∶2
D.t2时氨气与氢气的物质的量相同
(3)对于Ⅱ所代表的物质,其逆反应速率最大的点是________(填“c”、“d”或“g”);对于Ⅰ所代表的物质,其正反应速率最小的点是________(填“a”、“e”或“f”).
(4)其他条件不变,只改变温度,在改变的这个温度下反应至t3时刻,此时n(H2)比图象中的值大,那么该温度最可能的是________.
A.673 K B.273 K
C.373 K D.1073 K
查看答案和解析>>
科目:高中化学 来源: 题型:
下列针对甲、乙、丙、丁四种实验及装置的说法,
不合理的是

A.甲可用来证明碳的非金属性比硅强
B.乙装置可用于碘水中碘的萃取及分液
C.用丙图示的方法检查此装置的气密性
D.丁装置:从①进气可收集NO;从②进气可收集NH3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com