
| A. | ①⑥⑦ | B. | ③⑤⑦ | C. | ③⑥⑦ | D. | ⑤⑥⑦ |
分析 产生氢气的量不变,则保证铁完全与盐酸反应;增大盐酸的浓度、升高温度、形成原电池、增大Fe与盐酸的接触面积都可以加快化学反应速率,据此分析.
解答 解:①加水,稀释了盐酸,故反应速率变慢,故不选;
②加入硝酸,不再生成氢气而是生成氮的氧化物,故不选;
③加浓盐酸,盐酸浓度增大,反应速率加快,故选;
④滴加硫酸铜溶液,铁把铜置换出来,形成原电池,故反应速率加快,但与盐酸反应的铁减少,故减少了产生氢气的量,故不选;
⑤加氯化钠固体,对反应速率无影响,故不选;
⑥升高温度,反应速率加快,故选;
⑦改用浓度大的盐酸,反应速率加快,故选;
故选C.
点评 本题考查了影响反应速率的因素.审题时要注意:加快反应速率和不改变氢气的量.


科目:高中化学 来源: 题型:选择题
| A. | SiH4的沸点高于CH4,可推测PH3的沸点高于NH3 | |
| B. | CO2晶体是分子晶体,可推测SiO2晶体也是分子晶体 | |
| C. | C2H6是碳链为直线型的非极性分子,可推测C3H8也是碳链为直线型的非极性分子 | |
| D. | NH4+为正四面体结构,可推测 PH4+ 也为正四面体结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氟一氯甲院 (CHClF2)中所有原子最外层都达到了8电子稳定结构 | |
| B. | “塑料王”不能使酸性高锰酸钾溶液褪色 | |
| C. | 四氟乙烯 (CF2=CF2)中所有的原子都在同一个平面上 | |
| D. | 三氯甲烷(CHCl3)可以用甲院与氯气的取代反应来制取 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
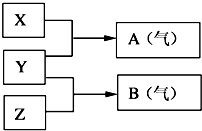 Ⅰ:A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为39,B、W 同周期,A、D同主族,A、W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等.
Ⅰ:A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为39,B、W 同周期,A、D同主族,A、W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等.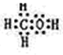 .
.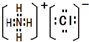 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | V(H2O)=0.003mol/(L•S) | B. | V(NH3)=0.003mol/(L•S) | ||
| C. | V(NH3)=0.002mol/(L•S) | D. | V(O2)=0.005mol/(L•S) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A组 | B组 |
| Ⅰ.H-I键键能大于H-Cl键键能 Ⅱ.H-I键键能小于H-Cl键键能 Ⅲ.HI分子间作用力大于HCl分子间作用力 Ⅳ.HI分子间作用力小于HCl分子间作用力 | ①HI比HCl稳定 ②HI比HCl不稳定 ③HI沸点比HCl高 ④HI沸点比HCl低 |
| A. | Ⅰ、① | B. | Ⅳ、② | C. | Ⅲ、③ | D. | Ⅱ、④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3:1 | B. | 3:2 | C. | 1:2 | D. | 6:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
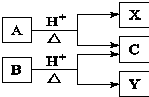 有机物A与B均由C、H、O组成,A与B互为同分异构体,在酸性条件下均可水解,只生成两种有机物.转化关系如图所示.下列有关说法中正确的是( )
有机物A与B均由C、H、O组成,A与B互为同分异构体,在酸性条件下均可水解,只生成两种有机物.转化关系如图所示.下列有关说法中正确的是( )| A. | X、Y一定互为同系物 | B. | X、Y的通式一定不同 | ||
| C. | X、Y可能互为同分异构体 | D. | X、Y一定互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过量的SO2通入NaOH溶液中:SO2+2OH-═SO32-+H2O | |
| B. | Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-═2Fe2++I2 | |
| C. | 酸性条件下,向含铬废水中加入FeSO4,可将Cr2O72-还原为Cr3+:Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O | |
| D. | NaHCO3溶液中加入过量的Ba(OH)2溶液:2HCO3-+Ba2++2OH-═BaCO3↓+2H2O+CO32- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com