
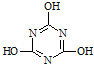
 +H2O下列有关三聚氰酸的说法正确的是( )
+H2O下列有关三聚氰酸的说法正确的是( )| A、分子式为C3H6N3O3 |
| B、分子中既含极性键,又含非极性键 |
| C、属于共价化合物 |
| D、生成该物质的上述反应为中和反应 |


 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案科目:高中化学 来源: 题型:
A、含18个中子的氯原子的核素符号:
| ||
B、比例模型 可以表示CO2 分子或SiO2分子 可以表示CO2 分子或SiO2分子 | ||
| C、HCO3-的电离方程式为:HCO3-+H2O?CO32-+H3O+ | ||
| D、次氯酸的结构式:H-Cl-O |
查看答案和解析>>
科目:高中化学 来源: 题型:
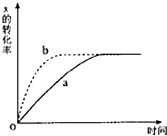 如图曲线a表示反应X(g)+Y(g)+N(s)?Z(g)+M(g)△H<0进行过程中X的转化率随时间变化的关系.若要改变起始条件,使反应过程按b曲线进
如图曲线a表示反应X(g)+Y(g)+N(s)?Z(g)+M(g)△H<0进行过程中X的转化率随时间变化的关系.若要改变起始条件,使反应过程按b曲线进| A、升高温度 |
| B、加大N的投入量 |
| C、缩小体积 |
| D、加大X的投入量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
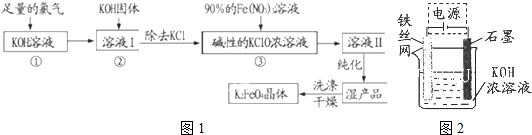
| 充电 |
| 放电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳酸氢钙溶液中加入过量氢氧化钠Ca2-+2HCO3-+2OH-=CaCO3↓+2H2O+CO32- |
| B、氧化铁可溶于氢碘酸:Fe2O3+6H+=2Fe2++3H2O |
| C、AlCl3溶液中加入过量的浓氨水:Al3++4NH3?H2O═AlO2-+2NH4++2H2O |
| D、Na2S溶液呈碱性:S2-+H2O=HS-+OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③④ | B、①② |
| C、②③ | D、③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①④⑥⑦ | B、②③⑤ |
| C、①③④⑤ | D、全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 丁 |
| 丁 |
| 甲 |
| A、若甲为C2H5OH,则丙可能为CH3COOH |
| B、若涉及反应均为氧化还原反应,则甲可能为Cl2 |
| C、若涉及反应均为氧化还原反应,则丁可能为O2 |
| D、若甲为AlCl3溶液,则丁可能是NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
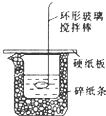 100mL0.55mol?L-1盐酸与100mL0.50mol?L-1氢氧化钠溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.试回答下列问题:
100mL0.55mol?L-1盐酸与100mL0.50mol?L-1氢氧化钠溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.试回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com