
ij�ܱ������м���0��3 mol A��0��1 mol C��һ������B�������塣һ�������·�����Ӧ��������Ũ����ʱ��仯��ͼ����ʾ��t0��t1�� c��B��δ�����ݡ�ͼ��Ϊt2��ı以����ͬ��ijһ������Ӧ������ʱ��仯�Ĺ�ϵͼ��t3��t4��ʹ���˴���������˵��������ǣ� ��
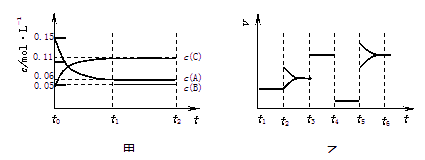
A���� t1��15 s��������C�� t0��t1ʱ��ε�ƽ����Ӧ����Ϊ 0��004mol��L��1��s��1
B��t4��t5�θı������Ϊ��Сѹǿ��t5��t6�ı������������ѧ��Ӧ���¶�
C��B����ʼ���ʵ���Ϊ0��02mol
D���û�ѧ��Ӧ�ı���ʽΪ��3A ![]() B + 2C
B + 2C

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����



 ��1��A����ʼ���ʵ���Ϊ
��1��A����ʼ���ʵ���Ϊ�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| Cu2O |
| ʱ��/min | 20 | 40 | 60 | 80 |
| n��O2��/mol | 0.0010 | 0.0016 | 0.0020 | 0.0020 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| t | 2 |
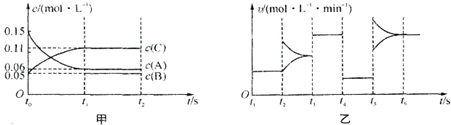
| A����t0=15 s������C��Ũ�ȱ仯��ʾ��t0��t1�ε�ƽ����Ӧ����Ϊ0.004mol?L-1?s-1 |
| B��t4��t5�θı������һ��Ϊ��Сѹǿ |
| C�����������ݻ�Ϊ2 L��B����ʼ���ʵ���Ϊ0.02 mol |
| D��t5��t6��Σ�������A�����ʵ���������0.03 mol�����˹����������������Ƚ�������Ϊa kJ���÷�Ӧ���Ȼ�ѧ����ʽΪ3A��g��?B��g��+2C��g����H=+100akJ?mol-1 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com