
| A. | AI溶解于氢氧化钠溶液中 | B. | Na与水反应 | ||
| C. | Na2O2与水反应 | D. | Fe与水蒸气在高温下反应 |
分析 水既不是氧化剂又不是还原剂,则在反应中,水所含的H元素和O元素的化合价没有发生变化,氧化还原反应中有元素的化合价发生变化,以此解答该题.
解答 解:A.AI溶解于氢氧化钠溶液中,水被还原生成氢气,水为氧化剂,故A错误;
B.Na与水反应生成NaOH和H2,H元素的化合价降低,水被还原,为氧化剂,故B错误;
C.Na2O2与水反应生成氢氧化钠和O2,只有氧元素的化合价发生变化,水既不是氧化剂又不是还原剂,故C正确;
C.Fe与水蒸气在高温下反应生成四氧化三铁和氢气,H元素的化合价降低,水被还原,为氧化剂,故D错误.
故选C.
点评 本题考查氧化还原反应,为高频考点,侧重于学生的分析能的考查,题目难度不大,注意根据物质的性质判断所发生的反应,注意元素化合价的变化.


 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案科目:高中化学 来源: 题型:选择题
| A. | K+、OH-、Na+、CO32- | B. | Cl-、Na+、Ag+、NO3- | ||
| C. | Fe3+、Cl-、Na+、OH- | D. | NH4+、Cl-、Na+、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①⑤⑦ | B. | ①②⑤⑦ | C. | ①②④⑤⑦ | D. | ②③④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油是各种液态烃的混合物 | |
| B. | 常压分馏的原料是重油 | |
| C. | 由分馏塔分馏出的各馏分均是混合物 | |
| D. | 减压分馏的主要产品有汽油、润滑油、煤油和沥青 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入氯化钡溶液产生白色沉淀,一定含有SO42- | |
| B. | 取溶液进行焰色反应是黄色,一定含有Na+ | |
| C. | 加入碳酸钠溶液产生白色沉淀,一定含有Ca2+ | |
| D. | 加入稀盐酸产生无色气体,一定含有CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Si→SiO2→H2SiO4→Na2SiO3 | B. | Fe→FeCl2→FeCl3→Fe(OH)3 | ||
| C. | Na→Na2CO2→Na2O2→NaOH | D. | Al→Al2O3→Al(OH)3→NaAlO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  检验Na2CO3 中的Na+ | B. |  除去CO中混有的CO2 | ||
| C. | 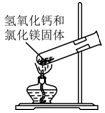 制取氨气 | D. |  吸收氨气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com