
下列有关叙述中正确的是( )
|
| A. | 难溶于水的电解质一定是弱电解质 |
|
| B. | 强电解质在水溶液中的电离过程是不可逆的 |
|
| C. | 易溶于水的电解质一定是强电解质 |
|
| D. | 强电解质的水溶液导电能力一定比弱电解质水溶液的导电能力强 |
考点:
弱电解质在水溶液中的电离平衡.
专题:
电离平衡与溶液的pH专题.
分析:
电解质的强弱与溶解性无关,强电解质在溶液中完全电离,弱电解质部分电离,溶液离子浓度越大,导电性越强,与电解质的强弱无关,以此解答该题.
解答:
解:A.难溶于水的电解质不一定为弱电解质,如硫酸钡、氯化银等难溶于水,但为强电解质,故A错误;
B.强电解质在溶液中完全电离,不存在电离平衡,故B正确;
C.电解质的强弱与溶解性无关,如HF易溶于水,但为弱电解质,故C错误;
D.溶液离子浓度越大,导电性越强,与电解质的强弱无关,如硫酸钡为强电解质,但难溶于水,溶液导电性较差,故D错误.
故选B.
点评:
本题考查电解质的强弱以及溶液的导电性的关系,为高频考点,侧重于基本概念的综合理解和运用的考查,难度不大.


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:
已知:2Fe2++Br2═2Fe3++2Br﹣,2Fe3++2I﹣═2Fe2++I2.向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.下列有关说法中,不正确的是( )
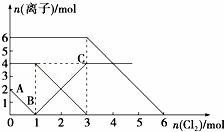
A. 还原性:I﹣>Fe2+>Br﹣
B. 原混合溶液中FeBr2的物质的量为6 mol
C. 当通入2 mol Cl2时,溶液中已发生的离子反应可表示为:2Fe2++2I﹣+2Cl2═2Fe3++I2+4Cl﹣
D. 原溶液中:n(Fe2+):n(I﹣):n(Br﹣)=2:1:3
查看答案和解析>>
科目:高中化学 来源: 题型:
雾霾会影响人们的生活与健康.某地区的雾霾中可能含有如下可溶性无机离子:Na+、NH4+、Mg2+、Al3+、SO42﹣、NO3﹣、Cl﹣.某同学收集了该地区的雾霾,经必要的预处理后得试样溶液,设计并完成了如下的实验:
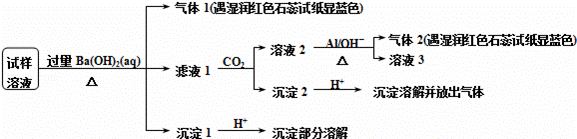
已知:3NO3﹣+8Al+5OH﹣+2H2O 3NH3↑+8AlO2﹣
3NH3↑+8AlO2﹣
根据以上的实验操作与现象,该同学得出的结论错误的是()
A. 试样中肯定存在NH4+、Mg2+、SO42﹣和NO3﹣
B. 试样中可能存在Na+、Cl﹣
C. 试样中一定不含Al3+
D. 可以确定该雾霾的成分是NaNO3、NH4Cl和MgSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
化合物A有稳定性好、抗氧化能力强的特点,其结构如图 .分子中片段X对A的性能起了重要作用,为研究X的结构,将化合物A在一定条件下水解只得到B(
.分子中片段X对A的性能起了重要作用,为研究X的结构,将化合物A在一定条件下水解只得到B(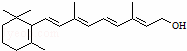 )和C.经测定确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,跟NaHCO3溶液反应有CO2产生
)和C.经测定确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,跟NaHCO3溶液反应有CO2产生
完成下列填空:
(1)化合物B能发生下列哪种类型的反应
a.取代反应b.加成反应c.缩聚反应d.氧化反应
(2)化合物C能经下列反应得到G(分子式为C8H6O2,分子内含五元环).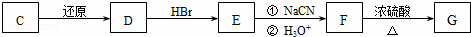
已知:ROOH RCH2OH RX
RCH2OH RX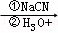 RCOOH
RCOOH
化合物C的结构简式为 .
(3)反应F→G的化学方程式为
(4)化合物E有多种同分异构体,1H核磁共振谱图表明,其中某些同分异构体含有苯环,且苯环上有两种不同化学环境的氢,写出这些同分异构体中任意三种的结构简式、、.
查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器中,一定条件下进行如下反应:NO(g)+CO(g)⇌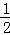 N2(g)+CO2(g)△H=﹣373.2kJ•mol﹣1,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
N2(g)+CO2(g)△H=﹣373.2kJ•mol﹣1,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
|
| A. | 加催化剂同时升高温度 | B. | 加催化剂同时增大压强 |
|
| C. | 升高温度同时充入N2 | D. | 降低温度同时减小压强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
利用“化学蒸气转移法”制备TaS2晶体,某温度下的2L恒容密闭容器中加入一定量 的 I2(g)和TaS2(s)发生如下反应:TaS2(s)+2I2(g)⇌TaI4(g)+S2(g)△H=a kJ•mol﹣1 (Ⅰ)达平衡时,TaS2(s)、I2(g)、TaI4(g)、S2(g)的物质的量分别为3mol、2mol、2mol、2mol.
(1)反应(Ⅰ)的平衡常数表达式K=
(2)若该温度下该容器中某时刻TaS2(s)、I2(g)、TaI4(g)、S2(g)的物质的量分别为2mol、2mol、4mol、4mol,则该时刻平衡向 (填“正反应”或“逆反应”)移动,v正 v逆(填“>”、“=”或“<”).
(3)在不同温度下,该反应的平衡常数K如下表:
| 温度/℃ | 40 | 80 | 200 |
| 平衡常数K | 1 | 1.5 | 4 |
该反应的△H 0(填“>”、“=”或“<”).
(4)40℃时,向该恒容密闭容器中加入2mol I2(g)和4mol TaS2(s),I2(g)的平衡转化率为 写出计算过程,结果保留小数点后1位)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
-A.-将氯化铁饱和溶液逐滴滴入氢氧化钠稀溶液中,边滴边搅拌,可获得氢氧化铁胶体
-B.-不能用乙醇萃取碘水中的碘是因为碘在水中溶解度比在乙醇中大
-C.-实验室可通过蒸馏的方法除去自来水中含有的氯离子等杂质制蒸馏水
-D.-浓硫酸不慎溅到皮肤上,应该立即用大量水冲洗,然后涂上稀NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作均要用玻璃棒,其中玻璃棒用作引流的是( )
①过滤 ②蒸发 ③溶解 ④向容量瓶转移液体.
|
| A. | ①和② | B. | ①和③ | C. | ③和④ | D. | ①和④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com