
 CH3OH(g) △H1=-116 kJ·mol-1
CH3OH(g) △H1=-116 kJ·mol-1| A.体系压强保持不变 |
| B.混合气体的密度保持不变 |
| C.CO与H2的浓度之比为1∶2 |
| D.单位时间内,消耗2molH2的同时消耗1mol CH3OH |
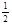 O2(g)=CO2(g) △H2=-283 kJ·mol-1 H2(g)+
O2(g)=CO2(g) △H2=-283 kJ·mol-1 H2(g)+ 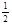 O2(g)=H2O(g) △H3=-242 kJ·mol-1
O2(g)=H2O(g) △H3=-242 kJ·mol-1 CO2(g)+2H2O(g) △H=-651kJ·mol-1 (2分)
CO2(g)+2H2O(g) △H=-651kJ·mol-1 (2分) CH3OH(g)
CH3OH(g) CO2(g)+2H2O(g) △H=—△H1+△H2+2△H3
CO2(g)+2H2O(g) △H=—△H1+△H2+2△H3

 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:高中化学 来源:不详 题型:单选题
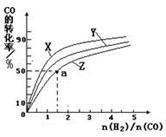
| 物质 | X | Y | Z |
| 初始浓度(mol/L) | 0.1 | 0.2 | 0 |
| 平衡浓度(mol/L) | 0.05 | 0.05 | 0.1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2Fe(s)+3CO2(g),其化学平衡常数K和温度t的关系如下表:
2Fe(s)+3CO2(g),其化学平衡常数K和温度t的关系如下表:| t℃ | 1000 | 1150 | 1300 |
| K | 64.0 | 50.7 | 42.9 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
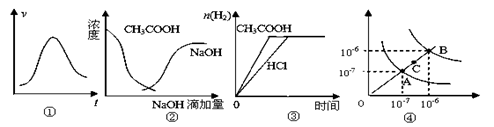
| A.图①表示一定条件下某化学反应的速率随时间变化的趋势图,该反应一定为放热反应 |
| B.图②中曲线表示将氢氧化钠溶液滴加到醋酸溶液浓度的变化趋势图 |
| C.图③表示等体积、等物质的量浓度的盐酸和醋酸溶液,分别加入足量镁粉,产生H2的物质的量的变化 |
| D.图④为水的电离平衡曲线图,若从A点到C点,可采用在水中加入适量NaOH固体的方法 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2C(g)+xD(s)的化学平衡状态,相关数据如下:M:3 mol A 、2 mol B;2 min达平衡,生成D 1.2 mol,测得从反应开始到平衡C的速率为0.3 mol·(L·min)-1。N:2 mol C 、y mol D;达平衡时c(A)="0.6" mol·L-1。下列推断的结论中不正确的是
2C(g)+xD(s)的化学平衡状态,相关数据如下:M:3 mol A 、2 mol B;2 min达平衡,生成D 1.2 mol,测得从反应开始到平衡C的速率为0.3 mol·(L·min)-1。N:2 mol C 、y mol D;达平衡时c(A)="0.6" mol·L-1。下列推断的结论中不正确的是 查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 B(g) + C(g);ΔH = ?48.25 kJ/L
B(g) + C(g);ΔH = ?48.25 kJ/L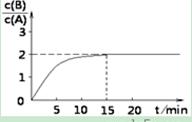
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2NO(g)+O2(g)△H>0,达到平衡。当改变其中一个条件X,Y随X的变化符合图中曲线的是
2NO(g)+O2(g)△H>0,达到平衡。当改变其中一个条件X,Y随X的变化符合图中曲线的是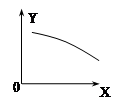
| A.X表示温度时,Y表示NO2物质的量 |
| B.X表示NO2物质的量,Y表示O2的物质的量 |
| C.X表示反应时间时,Y表示混合气体的密度 |
| D.X表示压强时,Y表示NO2的含量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2R(g) ΔH>0。在图中Y轴是指
2R(g) ΔH>0。在图中Y轴是指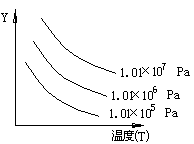
| A.平衡混合气中R的质量分数 | B.G的转化率 |
| C.平衡混合气中G的体积分数 | D.L的转化率 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
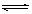 2SO3(气),已知反应过程中某一时SO2、O2、SO3,的浓度分别为0.2mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是
2SO3(气),已知反应过程中某一时SO2、O2、SO3,的浓度分别为0.2mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是| A.SO2为0.4mol/L、O2为0.2mol/L | B.SO3为0.4mol/L |
| C.SO2、S03均为0.15mol/L | D.SO2为0.25mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com