
下列分子的空间构型可用sp2杂化轨道来解释的是( )
①BF3 ②CH2===CH2 ③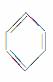 ④CH≡CH
④CH≡CH
⑤NH3 ⑥CH4
A.①②③ B.①⑤⑥
C.②③④ D.③⑤⑥
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:
下列关于金属的叙述中,不正确的是( )
A.金属键是金属阳离子和自由电子这两种带异性电荷的微粒间的强烈相互作用,其实质与离子键类似,也是一种电性作用
B.金属键可以看作是许多原子共用许多电子所形成的强烈的相互作用,所以与共价键类似,也有方向性和饱和性
C.金属键是带异性电荷的金属阳离子和自由电子间的相互作用,故金属键无饱和性和方向性
D.构成金属的自由电子在整个金属内部的三维空间中做自由运动
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.在含4 mol Si—O键的二氧化硅晶体中,氧原子的数目为4 NA
B.金刚石晶体中,碳原子数与C—C键数之比为1∶2
C.30 g二氧化硅晶体中含有0.5 NA个二氧化硅分子
D.晶体硅、晶体氖均是由相应原子直接构成的原子晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于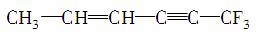 分子结构的叙述中,正确的是( )
分子结构的叙述中,正确的是( )
①6个碳原子可能都在一条直线上 ②6个碳原子不可能都在同一条直线上 ③6个碳原子可能都在同一平面上 ④6个碳原子不可能都在同一平面上
A.①③ B.②③
C.①④ D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
用价电子对互斥理论预测H2S和BF3的立体结构,两个结论都正确的是( )
A.直线形;三角锥形 B.V形;三角锥形
C.直线形;平面三角形 D.V形;平面三角形
查看答案和解析>>
科目:高中化学 来源: 题型:
0.5 mol A元素的最高价离子被还原成中性原子时,得到6.02×1023个电子,它的单质同盐酸充分反应时,放出0.02 g 氢气,用去0.4 g单质A。B元素的原子核外电子层数与A相同,且B元素形成的单质是深红棕色液体。
(1)写出两种元素的名称:A________,B________;
(2)用结构示意图表示两种元素的常见离子___________。
(3)指出A与B形成化合物的化学键的类型:
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
正误判断,正确的划“√”,错误的划“×”
(1)在常温常压下,32 g 18O2中含有2NA氧原子( )
(2)17 g —OH与17 g OH-所含电子数均为10NA( )
(3)相同质量的N2O4与NO2中所含原子数目相同( )
(4)m g CO与N2的混合气体中所含分子数目为 NA( )
NA( )
(5)4.5 g SiO2晶体中含有的硅氧键的数目为0.3NA( )
(6)30 g甲醛中含共用电子对总数为4NA( )
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com