

 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
| 物质 | 组成和结构信息 |
| a | 含有A、D两种元素的化合物分子中含有极性键和非极性键 |
| b | 化学组成为BDF2的化合物,其中B元素显其最高化合价 |
查看答案和解析>>
科目:高中化学 来源: 题型:
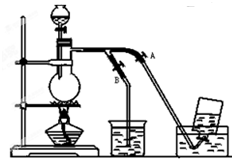 如图表示在没有通风处收集纯净的氯气时设计的装置图,图中A、B是可控制的弹簧铁夹.
如图表示在没有通风处收集纯净的氯气时设计的装置图,图中A、B是可控制的弹簧铁夹.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、O3+2KI+H2O═2KOH+I2+O2 |
| B、2CH3COOH(醋酸)+Ca(ClO)2═2HClO+(CH3COO)2Ca |
| C、I2+2NaClO3═2NaIO3+Cl2 |
| D、4HCl(浓)+MnO2=△=MnCl2+Cl2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应热就是反应中放出的能量 |
| B、在任何条件下,化学反应的焓变都等于化学反应的反应热 |
| C、由C(s,石墨)═C(s,金刚石)△H=+1.9kJ?mol-1可知,金刚石比石墨稳定 |
| D、等量的硫蒸气和硫固体分别完全燃烧,前者放出的热量多 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1g水中含氧原子数为 NA/18 |
| B、NA个CO2分子和NA个CO分子质量比为11:7 |
| C、18g水中含电子数为8NA个 |
| D、1mol Fe2+带2NA个正电荷 |
查看答案和解析>>
科目:高中化学 来源: 题型:
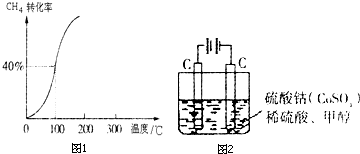
| 1 |
| 2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com