
【题目】下列关于乙烯的说法正确的是( )
A.能使溴水褪色B.易溶于水
C.结构简式为CH2CH2D.是天然气的主要成分
 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:
【题目】(1).FeCl3是中学实验室常用的试剂,可以用来制备氢氧化铁胶体。
下列制备氢氧化铁胶体的操作方法正确的是____________(填字母);
A.向饱和氯化铁溶液中滴加少量的氢氧化钠稀溶液
B.加热煮沸氯化铁饱和溶液
C.在氨水中滴加氯化铁浓溶液
D.在沸水中滴加饱和氯化铁溶液,煮沸至液体呈红褐色。
(2)写出Ba(OH)2溶液与少量NaHCO3溶液反应的离子方程式:___________________。
(3)写出次氯酸的电子式:________________;写出过氧化钠中存在的所有化学键类型:____________________。
(4)铁粉中含有铝粉,可加______除去杂质,发生的化学方程式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业废水中常含有一定量的Cr2O72-,易被人体吸收累积而导致肝癌。处理工业含铬废水的方法通常是将Cr2O72-转化为Cr3+,再将Cr3+转化为Cr(OH)3沉淀。已知元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr(OH)4(绿色)、Cr2O72(橙红色)、CrO42(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体。
(1)Cr3+与Al3+的化学性质相似,在Cr2(SO4)3溶液中逐滴加入NaOH溶液直至过量,可观察到的现象是____
(2)利用硫酸工业废气中的SO2可以处理酸性含铬废水,用离子方程式表示反应原理:_______________
(3)Cr3+在强碱中可被双氧水氧化为CrO42-,发生反应的离子方程式为_________________
(4)CrO42和Cr2O72在溶液中可相互转化。室温下,初始浓度为1.0 mol·L1 的Na2CrO4溶液中c(Cr2O72)随c(H+)的变化如图所示。
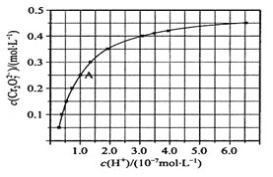
①由图可知,溶液酸性增大,CrO42的平衡转化率_________(填“增大“减小”或“不变”),
② 据A点数据,计算出该转化反应的平衡常数__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过海水晾晒可以得到粗盐,粗盐除还有NaCl外,还含有MgCl2、 CaCl2、 Na2SO4以及泥沙等杂质。以下是某兴趣小组制备精盐的实验方案,各步操作流程如下。下列说法正确的是

A. 实验过程中①、⑤步骤的操作分别是溶解、过滤
B. 实验过程中步骤④的目的是仅除去溶液中的Ca2+
C. 实验过程中步骤⑦中的蒸发所用到的仪器是酒精灯、玻璃棒、烧杯、铁架台(带铁圈)
D. 实验过程中②、④步骤互换,对实验结果不影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A是基本的有机化工原料,A与CO、H2O以物质的量1:1:1的比例生成B。B、C两物质中的官能团分别具有乙酸、乙醇中官能团的性质。D是有芳香味、不溶于水的油状液体。有关物质的转化关系如下:

请回答:
(1)A的结构简式______________________________
(2)B + C → D的化学方程式____________________________________________________________
(3)下列说法不正确的是 ___________________
A.有机物A能使酸性高锰酸钾溶液褪色
B.有机物B与乙酸互为同系物
C.有机物B、C都能与金属钠反应,且等物质的量的B、C与足量钠反应产生氢气质量相等
D.可用NaOH溶液来除去有机物D中混有的杂质B
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某二元酸(H2A)在水溶液中的电离方程式是:H2A=H++HA-;HA-![]() H++A2-,回答下列问题:
H++A2-,回答下列问题:
(1)Na2A溶液显___(填“酸性”、“中性”或“碱性”),理由是____(用离子方程式表示);NaHA溶液显____(填“酸性”、“中性”或“碱性”),理由是_____(用离子方程式表示)。
(2)若0.1 mol·L-1NaHA溶液的pH=2,则0.1 mol·L-1H2A溶液中c(H+)________(填“>”、“=”或“<”)0.11 mol·L-1。
(3)0.1 mol·L-1NaHA溶液中各种离子浓度由大到小的顺序是__________________。
(4)H2A溶液和Na2A溶液能否发生反应?若能反应请写出离子方程式:______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如右,电解总反应为:2Cu+H2O![]() Cu2O+H2↑。下列说法正确的是
Cu2O+H2↑。下列说法正确的是

A. 石墨电极上产生氢气
B. 铜电极发生还原反应
C. 铜电极接直流电源的负极
D. 当有0.1 mol电子转移时,有0.1 mol Cu2O生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以赤铁矿为原料,利用高炉炼铁的基本反应为:
i.Fe2O3(s)+3CO![]() 2Fe(s)+3CO2(g)△H1
2Fe(s)+3CO2(g)△H1
其中CO产生的反应是:
ii.C(焦炭,s)+O2(空气,g)=CO2(g)△H2<0
iii.C(焦炭,s)+CO2(g)=2CO(g)△H3>0
(1)以焦炭炼铁的反应:3C(焦炭,s)+2Fe2O3(s)![]() 4Fe(s)+3CO2(g)的△H=____________(请用含△H1、△H2或H3的式子表示)。
4Fe(s)+3CO2(g)的△H=____________(请用含△H1、△H2或H3的式子表示)。
(2)反应i的平衡常数与温度的关系如下表,请回答:
温度/℃ | 1000 | 1150 | 1300 |
平衡常数K | 64.0 | 50.6 | 42.9 |
①当反应温度为1150℃,高炉中n(CO):n(CO2)=4:1时,v正_____v逆(填大于、小于、或等于)。
②己知高炉容积VL,反应温度1000℃。若提供给i反应的CO共2.24×103L(已折算标准状况),该反应经过tmin达平衡,则CO2在此段时间的反应速率为________(用V、t代数式表示)。
(3)T℃下,初始体积均为2L,初始压强均为100kPa的甲(固定体积),乙(固定压强)两容器中各充入2molCO进行反应iii,达平衡时甲中气体压强变为原来的4/5倍。请回答:
①下列可以判断甲中反应达平衡的是________________(填字母序号)。
a.2c(CO2)=c(CO)
b.v正(CO2)=2v逆(CO)
c.气体密度不再改变
d.气体平均分子量不再改变
②下图为甲、乙两容器中CO的百分含量(CO%)与时间(t)的关系示意图,其中代表乙容器的是___________(填字母编号),理由是______________________。

③乙容器中达平衡时的平衡常数Kp=___________________(Kp为用压强表达的平衡常数)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com