
【题目】用如图装置进行实验,将液体A逐滴加入到固体B中,下列叙述正确的是
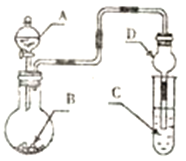
A. 若A为浓热酸,B为MnO2,C中盛有I2淀粉溶液,C中溶液变蓝色
B. 若A为H2O2,B为MnO2,C中盛有Na2S溶液,C中溶液变浑浊
C. 若A为浓氨水,B为生石灰,C中盛有AlCl3溶液,C中先产生白色沉淀后沉淀又溶解
D. 若A为浓H2SO4,B为CaCO3,C中盛有Na2SiO3溶液,C中溶液出现白色沉淀,证明非金属性S>C>Si
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
【题目】下列关于有机化合物说法正确的是
A. 有机物![]() 的名称是2,3,5,5-四甲基-4-乙基己烷
的名称是2,3,5,5-四甲基-4-乙基己烷
B. 乙酸乙酯在碱性条件下的水解反应称为皂化反应
C. 有机物![]() 中可能共面的原于数最多有17个
中可能共面的原于数最多有17个
D. 乙醛和丙烯醛(![]() )不是同系物,分别与足量H2反应后的产物也不是同系物
)不是同系物,分别与足量H2反应后的产物也不是同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为验证还原性:SO2>Fe2+>C1-,三组同学分别进行了下图实验,并对溶液1和溶液2中所含离子进行了检验,能证明上述还原性顺序的实验组有
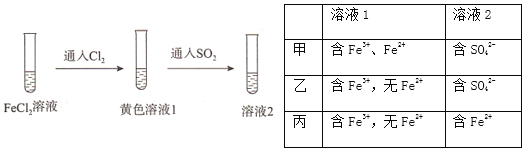
A. 只有甲 B. 甲、乙 C. 甲、丙 D. 甲、乙、丙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求回答下列问题:
Ⅰ.写出下列物质或微粒的电子式:
(1)CO2________
(2)N2___________
(3)Na2O__________
Ⅱ.下列物质:① CaBr2②H2O③NH4Cl④H2O2⑤Na2O2⑥Ca(OH)2⑦HClO⑧I2⑨He
(1)含有共价键的离子化合物是(用序号回答)________
(2)当其熔化时,不破坏化学键的是(用序号回答)_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醛(HCHO)俗称蚁醛,是一种重要的有机原料。
I.利用甲醇(CH3OH)制备甲醛
脱氢法:CH3OH(g)=HCHO(g)+H2(g) △H1 = +92.09kJ/mol
氧化法:CH3OH(g) +1/2O2(g)=HCHO(g)+H2O(g) △H2
(1)已知:2H2(g)+O2(g)=2H2O(g) △H3=-483.64 kJ/mol,则△H2=_______。
(2)与脱氢法相比,氧化法在热力学上趋势较大,其原因为_______________。
(3)图1为甲醇制备甲醛反应的lg K(K为平衡常数)随温度(T)的变化曲线。曲线____(填“a”或“b”)对应脱氢法,判断依据为_________________。

II.甲醛的用途
(4)将甲醛水溶液与氨水混合蒸发可制得乌洛托品(结构简式如图2),该物质在医药等工业中有广泛用途。若原料完全反应生成乌洛托品,则甲醛与氨的物质的量之比为_______。
(5)将甲醛水溶液与硫酸镍(NiSO4)混合,可用于化学镀镍。若反应过程中有CO2产生,则该反应的离子方程式为____________________。
Ⅲ.甲醛的检测
(6)室内甲醛超标会危害人体健康,通过传感器可以监测空气中甲醛的含量。一种燃料电池型甲醛气体传感器的原理如图3所示,则b极的电极反应式为_________,当电路中转移4×10-4 mol电子时,传感器内参加反应的HCHO为_______mg。
查看答案和解析>>
科目:高中化学 来源: 题型:
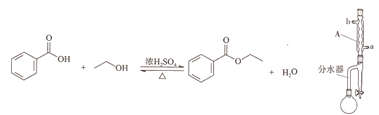
【题目】实验室制备苯甲酸乙酯的反应装置示意图和有关数据如下:
相对分子质量 | 密度/(g/cm3) | 沸点/℃ | 水中溶解性 | |
苯甲酸 | 122 | 1.266 | 249 | 微溶 |
乙醇 | 46 | 0.789 | 78.3 | 溶 |
苯甲酸乙酯 | 150 | 1.045 | 213 | 难溶 |
环己烷 | 84 | 0.779 | 80.8 | 难溶 |
环已烷、乙醇和水可形成共沸物,其混合物沸点为62.1℃。
合成反应:向圆底烧瓶中加入6.1g苯甲酸、20mL无水乙醇、25mL环已烷和2片碎瓷片,搅拌后再加入2mL浓硫酸。按图组装好仪器后,水裕加热回流1.5小时。
分离提纯:继续水浴加热蒸出多余乙醇和环已烷,经分水器放出。剩余物质倒入盛有60mL冷水的烧怀中,依次用碳酸钠、无水氯化钙处理后,再蒸馏纯化,收集210~213℃的馏分。得产品5.0g。
回答下列问题:
(1)仪器A的名称为_______,冷却水应从______(填“a”或“b”)口流出。
(2)加入环己烷的目的为______________。
(3)合成反应中,分水器中会出现分层现象,且下层液体逐渐增多,当下层液体高度超过距分水器支管约2cm时开启活塞放出少量下层波体。该操作的目的为_________________。
(4)实验中加入碳酸钠的目的为__________;经碳酸钠处理后,若粗产品与水分层不清,可采取的措施为___________(填字母)。
(5)在该实验中,圆底烧瓶的容积最适合的是_____。
A.50mL B.100mL C.200mL D.300mL
(6)本实验的产率为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有5种短周期元素的原子序数按E、D、B、A、C 的顺序依次增大; A、C 同周期,B、C同主族;A 与B 可形成离子化合物A2B,A2B 中阴阳离子的电子层结构完全相同,且电子总数为30;D 和E可形成4 核10 电子的分子。试回答下列问题:
(1)写出这5种元素的名称: A______B______C______D______E______
(2)写出下列物质的电子式:
①D 元素形成的单质___________ ②B 与E 形成的四原子化合物________
③A.B、E 形成的化合物__________ ④D、E 形成的简单化合物__________
(3)B、D、E形成的原子个数3:2:4的盐的化学式为_______,类别属于______化合物(填离子或共价),含有的化学键类型__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com