
| A. | Q1=Q2=Q3 | B. | Q3<Q1<Q2 | C. | Q3<Q2<Q1 | D. | Q1<Q2<2Q3 |
分析 反应放出热量越大,Q的数值越大;反应物计量数越大,放热热量越大;液态水具有能量较低,生成物为液态水时放出热量越大,据此进行判断.
解答 解:①2H2(g)+O2(g)=2H2O(g)+Q1kJ;
②2H2(g)+O2(g)=2H2O(l)+Q2kJ;
③H2(g)+$\frac{1}{2}$O2(g)=H2O(g)+Q3kJ;
反应③中计量数为①②的$\frac{1}{2}$,则反应③放出的热量最小,即Q3最小;
反应①②中,反应①生成气体水、反应②生成液态水,气体水具有能量较高,则反应②放出的热量大于反应③,即Q1<Q2,
所以放出热量Q1、Q2、Q3的大小关系为:Q3<Q1<Q2,
故选B.
点评 本题考查了反应热大小比较,题目难度不大,明确物质状态与反应热的关系为解答关键,注意掌握影响反应热的因素,试题侧重基础知识的考查,培养了学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 铝制电线电缆 | B. | 铝制餐具 | C. | 铝制可乐易拉罐 | D. | 糖果内包装 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
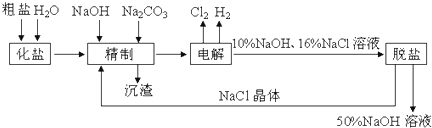
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | ②、⑧、⑨对应简单离子半径依次减小 | |
| B. | ⑤的三种核素化学性质不同 | |
| C. | 元素=10 ⑩处于常见周期表第四周期第VIIIB族 | |
| D. | ④的最高价氧化物对应的水化物能与其氢化物反应,生成离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化钠的电子式: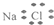 | B. | 中子数为20的氯原子:${\;}_{17}^{20}$Cl | ||
| C. | NH3的电子式: | D. | S2-的结构示意图: |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,F
,F ,AB2
,AB2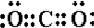 ,A的最简单气态氢化物
,A的最简单气态氢化物 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤⑧ | B. | ②④⑥⑧ | C. | ③⑤⑦ | D. | ⑤⑥⑦ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com