
| A. | Na+ H+ NO3- HCO3- | B. | Fe2+ H+ Cl- NO3- | ||
| C. | Fe3+ Ca2+ OH- NO3- | D. | Ba2+ Na+ OH-NO3- |
分析 A.氢离子与碳酸氢根离子反应生成二氧化碳气体,该反应不属于氧化还原反应;
B.硝酸根离子在酸性条件下具有强氧化性,能够氧化亚铁离子;
C.铁离子、钙离子与氢氧根离子反应,但该反应不属于氧化还原反应;
D.四种离子之间不发生反应,能够大量共存.
解答 解:A.H+、HCO3-之间反应生成二氧化碳气体和水,但不反应不是氧化还原反应,故A错误;
B.Fe2+、H+、NO3-之间发生氧化还原反应,在溶液中不能共存,故B正确;
C.Fe3+、Ca2+都与OH-发生反应,在溶液中不能大量共存,该反应不属于氧化还原反应,故C错误;
D.Ba2+、Na+、OH-、NO3-之间不反应,在溶液中能够大量共存,故D错误;
故选B.
点评 本题考查离子共存的判断,题目难度不大,注意明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间,能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;试题侧重基础知识的考查,有利于培养学生的灵活应用能力.


 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:高中化学 来源: 题型:选择题
| A. | 将NaOH浓溶液滴加到饱和FeCl3溶液中制备Fe(OH)3胶体 | |
| B. | 用向上排空气法收集铜粉与稀硝酸反应产生的NO | |
| C. | 配制氯化铁溶液时,将氯化铁溶解在较浓的盐酸中再加水稀释 | |
| D. | 将Cl2与HCl混合气体通过饱和食盐水可得到纯净的Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
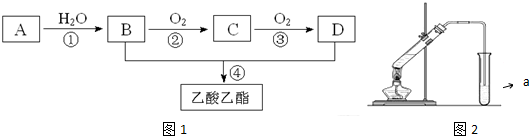
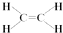 ,C的结构简式:CH3CHO.
,C的结构简式:CH3CHO.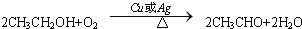 ;反应类型:氧化反应.
;反应类型:氧化反应.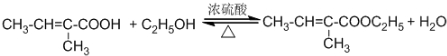 ,为从该实验后的混合气体中分离出乙酸乙酯,右侧试管中所选用的试剂a是饱和碳酸钠溶液,a试剂的作用是中和乙酸、吸收乙醇、降低乙酸乙酯在溶液中的溶解度,有利于分层析出.
,为从该实验后的混合气体中分离出乙酸乙酯,右侧试管中所选用的试剂a是饱和碳酸钠溶液,a试剂的作用是中和乙酸、吸收乙醇、降低乙酸乙酯在溶液中的溶解度,有利于分层析出.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
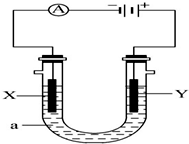 电解原理在化学工业中有广泛应用.如图表示一个电解池,X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞溶液,请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞溶液,请回答以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
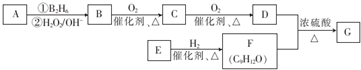
 ;该反应的反应类型为取代反应或酯化反应
;该反应的反应类型为取代反应或酯化反应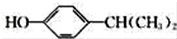 .
.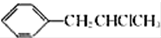 为原料也可合成F,请参考题目中的相关信息写出相应的合成路线图(反应条件中的试剂写在箭头上方,其他写在箭头下方):
为原料也可合成F,请参考题目中的相关信息写出相应的合成路线图(反应条件中的试剂写在箭头上方,其他写在箭头下方):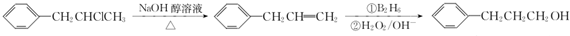 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
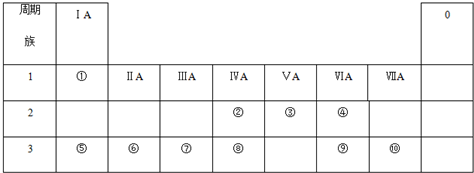
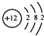
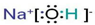
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com