
| 3mol×6mol |
| 6mol |
| 2mol×6mol |
| 6mol |
| 44.8L×6mol |
| 6mol |
| 8mol |
| 2L |


科目:高中化学 来源: 题型:
 马踏飞燕--是我国的旅游标志如图,出土的马踏飞燕是由表铜制成,下列有关该标志的叙述不正确的是( )
马踏飞燕--是我国的旅游标志如图,出土的马踏飞燕是由表铜制成,下列有关该标志的叙述不正确的是( )| A、青铜硬度比纯铜的硬度小 |
| B、青铜的主要成分是Cu、Sn、Pb等 |
| C、出土于东汉晚期 |
| D、青铜是我国使用最早的合金 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙酸与碳酸钙固体反应的离子方程式:2H++CaCO3=Ca2++CO2↑+H2O |
B、苯酚钠溶液中通入少量二氧化碳的离子方程式: |
C、制备酚醛树脂的化学方程式: |
D、丙烯聚合成聚丙烯的化学方程式: |
查看答案和解析>>
科目:高中化学 来源: 题型:
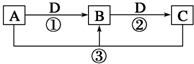 已知A、B、C、D是中学化学的常见物质,且A、B、C均含有同一种元素.在一定条件下它们之间的相互转化关系如图所示(部分反应中的H2O已略去).
已知A、B、C、D是中学化学的常见物质,且A、B、C均含有同一种元素.在一定条件下它们之间的相互转化关系如图所示(部分反应中的H2O已略去).查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com