
��֪ij��ѧʵ��Ľ�����±���
| ʵ����� | ��Ӧ�� | ����ͬ�¶��²�õķ�Ӧ����v/mol·L��1·min��1 | |
| ��С��ͬ�Ľ���Ƭ | ����Һ | ||
| 1 | þ�� | 1 mol·L��1���� | v1 |
| 2 | ��Ƭ | 1 mol·L��1���� | v2 |
| 3 | ��Ƭ | 0.1 mol·L��1���� | v3 |
���н�����ȷ����(����)
A��v1��v2��v3 B��v3��v2��v1
C��v1��v3��v2 D��v2��v3��v1
 ��ĩ���䵥Ԫ�����ิϰ��ϵ�д�
��ĩ���䵥Ԫ�����ิϰ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ʵ�飺��0.1 mol·L��1MgCl2��Һ��0.2 mol·L��1NaOH��Һ�������ϵõ���Һa��ȡ������Һa���˵õ���Һb�Ͱ�ɫ����c��������Һa�еμ�0.1 mol·L��1FeCl3��Һ�����ֺ��ɫ���������з�������ȷ����(����)
A��Һb��pH��7
B��������ɫ�仯˵��Mg(OH)2ת��ΪFe(OH)3
C��ʵ�����֤��Fe(OH)3���ܽ�ȱ�Mg(OH)2��С
D����Һa�д��ڳ����ܽ�ƽ�⣺Mg(OH)2(s)Mg2��(aq)��2OH��(aq)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ö�������(ClO2)���Ʊ���;�㷺����������(NaClO2)��ʵ���ҿ�������װ��(��ȥ���ּг�����)�Ʊ��������������ơ�
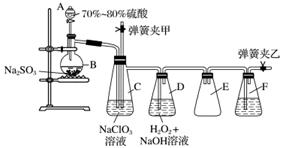
װ��C�з�����Ӧ��2NaClO3��SO2===2ClO2��Na2SO4(��)
װ��D�з�����Ӧ��2ClO2��H2O2��2NaOH===2NaClO2��2H2O��O2(��)
(1)������װ��ϣ��ر��������ɼУ���A�л�������A��ע��ˮ�ɼ���װ�������ԣ�װ�����������õ�������________________________��ʵ�鿪ʼʱ����A�Ļ������������ɼеĿ��ز�����__________________��F��ʢ�е�Һ��Ϊ________��
(2)װ��B�н��е��������������������Ʊ���������ķ�Ӧ���ô�ʹ�õ���70%��80%�����ᣬ������98%��Ũ�����ϡ�����ᣬԭ����___________________________________��
(3)װ��C��������________________��װ��E��������________________��
(4)�ڼ�����Һ��NaClO2�Ƚ��ȶ�������װ��D��Ӧά��NaOH�Թ������ж�NaOH�Ƿ��������Ҫ���Լ���________��
a��ϡ���� b��Ʒ����Һ c��ʯ����Һ d����̪��Һ
(5)һ��ʵ���Ʊ��У�ͨ�����鷢���Ʊ���NaClO2�к���NaOH��Na2SO3��������Щ���ʵĿ���ԭ����__________________����������к���Na2SO3���ʵ�ʵ�������������________________________________________________________________________��
(��ѡ����Լ��У�Ba(OH)2��Һ��H2O2��Һ��AgNO3��Һ��Ʒ����Һ��H2SO4��Һ)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ�������£�N2O�ֽ�IJ���ʵ���������£�
| ��Ӧʱ��/min | 0 | 10 | 20 | 30 | 40 | 50 |
| c(N2O)/mol·L��1 | 0.100 | 0.090 | 0.080 | 0.070 | 0.060 | 0.050 |
| ��Ӧʱ��/min | 60 | 70 | 80 | 90 | 100 | |
| c(N2O)/mol·L��1 | 0.040 | 0.030 | 0.020 | 0.010 | 0.000 |
��ͼ����ȷ��ʾ�÷�Ӧ�й��������仯���ɵ���(����)
(ע��ͼ�а�˥��ָ��һŨ��N2O����һ��ʱ�������Ӧʱ�䣬c1��c2����ʾN2O��ʼŨ����c1��c2)
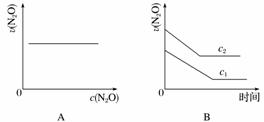
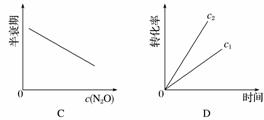
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵����ȷ����(����)
�ٲμӷ�Ӧ�����ʵ�������Ӱ�컯ѧ��Ӧ���ʵ���Ҫ����
�ڹ���Ӱ��ijЩ��ѧ��Ӧ���ʵ��������֮һ���۾�����ѧ��Ӧ���ʵ���Ҫ������Ũ�ȡ��ܲ���ʲô��Ӧ������Ũ�ȡ����ȡ���ѹ��ʹ�ô��������Լӿ췴Ӧ����
A���٢� B���ڢ� C���ۢ� D���٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
һ���¶��£���2 L�ĺ����ܱ������У�X��Y��Z������������ʵ�����ʱ��仯��������ͼ��ʾ��
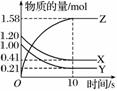
(1)�ӷ�Ӧ��ʼ��10 sʱ����Z��ʾ�ķ�Ӧ����Ϊ__________��X�����ʵ���Ũ�ȼ�����________��Y��ת����Ϊ______��
(2)�÷�Ӧ�Ļ�ѧ����ʽΪ______________________________________��
(3)10 s���ijһʱ��(t1)�ı��������������������ʱ��ı仯ͼ����ͼ��ʾ��������˵�����ϸ�ͼ�����______��
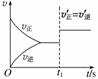
A��t1ʱ�̣�������X��Ũ��
B��t1ʱ�̣���������ϵ�¶�
C��t1ʱ�̣���С���������
D��t1ʱ�̣�ʹ���˴���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��Ũ��Ϊ0.1 mol·L��1 HF��Һ��ˮ����ϡ�ͣ����и���ʼ�ձ����������(����)
A��c(H��) B��Ka(HF)
C.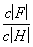 D.
D.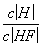
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ж�������ȷ�Ļ����̡�������Ļ�������
(1)25 ��ʱ���ô�����Һ�ζ���Ũ��NaOH��Һ��pH��7��V���VNaOH(����)
(2013·�������ۣ�2B)
(2)ϡ�����ˮϡ�ͣ�����ĵ���̶�������Һ��pH��С(����)
(2012·�������ۣ�10B)
(3)�к͵�����������ʵ���Ũ�ȵ�����ʹ��������ĵ�n(NaOH)���(����)
(2012·�������ۣ�10C)
(4)CH3COOH��Һ��ˮϡ�ͺ���Һ��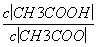 ��ֵ��С(����)
��ֵ��С(����)
(2013·���գ�11C)
(5)�����£�����0.10 mol·L��1�İ�ˮ����ˮϡ�ͺ���Һ��c(NH )·c(OH��)���(����)
)·c(OH��)���(����)
(2013·�������ۣ�8B)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
̼������������ѧ��ѧ��Ҫ�ķǽ���Ԫ�أ��ڹ�ũҵ�������й㷺��Ӧ�á�
 ��1�����ڷ��䡰�칬һ�š��ij������Ż����ȼ����Һ̬ƫ�����£�CH3��2N��NH2����������Һ̬�����������������ڷ�Ӧ�����зų�����������ͬʱ������������Ⱦ�����塣��֪�����£�1 gȼ����ȫȼ���ͷų�������Ϊ42.5kJ����д���÷�Ӧ���Ȼ�ѧ����ʽ________________________________________��
��1�����ڷ��䡰�칬һ�š��ij������Ż����ȼ����Һ̬ƫ�����£�CH3��2N��NH2����������Һ̬�����������������ڷ�Ӧ�����зų�����������ͬʱ������������Ⱦ�����塣��֪�����£�1 gȼ����ȫȼ���ͷų�������Ϊ42.5kJ����д���÷�Ӧ���Ȼ�ѧ����ʽ________________________________________��
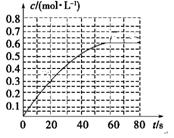
��2��298 Kʱ����2L���ܱ������У��������淴Ӧ��2NO2(g)
N2O4(g)����H����a kJ��mol��1 (a��0) ��N2O4�����ʵ���Ũ����ʱ���
����ͼ����ƽ��ʱ�� N2O4��Ũ��ΪNO2��2�����ش��������⡣
��298kʱ���÷�Ӧ��ƽ�ⳣ��Ϊ________��
�����¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯������ͼ��ʾ������˵����ȷ����
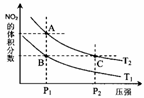 a��A��C����ķ�Ӧ���ʣ�A��C
a��A��C����ķ�Ӧ���ʣ�A��C
b��B��C����������ƽ����Է���������B��C
c��A��C�����������ɫ��A�Cdz
d����״̬B��״̬A�������ü��ȵķ���
������Ӧ��398K���У�ijʱ�̲��n��NO2��=0.6 mol n��N2O4��=1.2mol�����ʱV������ V���棩���>������<����=������
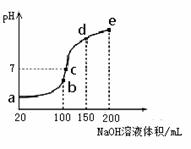 ��3��NH4HSO4�ڷ����Լ���ҽҩ�����ӹ�ҵ����;�㷺������100 mL 0.1 mol��L��1NH4HSO4��Һ�еμ�0.1 mol��L��1NaOH��Һ���õ�����ҺpH��NaOH��Һ����Ĺ�ϵ������ͼ��ʾ��
��3��NH4HSO4�ڷ����Լ���ҽҩ�����ӹ�ҵ����;�㷺������100 mL 0.1 mol��L��1NH4HSO4��Һ�еμ�0.1 mol��L��1NaOH��Һ���õ�����ҺpH��NaOH��Һ����Ĺ�ϵ������ͼ��ʾ��
�Է���ͼ��a��b��c��d��e����㣬
��ˮ�ĵ���̶�������__________��
������Һ��c(OH-)����ֵ��ӽ�NH3��H2O�ĵ��볣��K��ֵ���� ��
����c�㣬��Һ�и�����Ũ���ɴ�С������˳����_______ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com