
| A. | S(s,单斜)═S(s,正交)△H=+0.33kJ•mol?1,正交硫比单斜硫稳定 | |
| B. | 2H2(g)+O2(g)═2H2O(g);△H=-489.6kJ•mol-1,氢气的燃烧热为489.6kJ•mol-1 | |
| C. | 当镀锌铁制品的镀层破损时,镀层仍能对铁制品起到保护作用 | |
| D. | 锌锰干电池工作一段时间后碳棒变细 |
分析 A、能量越低越稳定;
B、燃烧热是1mol可燃物质完全燃烧生成稳定氧化物放出的热量;
C、Fe与Zn构成原电池时,Fe作正极被保护;
D、根据锌锰干电池的正极是碳棒,该极上二氧化锰发生得电子的还原反应.
解答 解:A、S(s,单斜)═S(s,正交)△H=+0.33kJ•mol?1,所以S(s,单斜)能量低稳定,故A错误;
B、燃烧热是1mol可燃物质完全燃烧生成稳定氧化物放出的热量,所以氢气的燃烧热应为1mol氢气燃烧生成液态水,故B错误;
C、Fe与Zn构成原电池时,Fe作正极被保护,所以当镀锌铁制品的镀层破损时,镀层能对铁制品起保护作用,故C正确;
D、在锌锰干电池中,正极是碳棒,该极上二氧化锰发生得电子的还原反应,该电极质量不会减少,故D错误;
故选C.
点评 本题考查了能量越低越稳定、燃烧热的定义以及金属的腐蚀与防护,侧重于基本概念的考查,题目难度不大.


科目:高中化学 来源: 题型:解答题
 在苹果、香蕉等水果的果香中存在着乙酸正丁酯.某化学课外兴趣小组欲以乙酸和正丁醇为原料合成乙酸正丁酯.
在苹果、香蕉等水果的果香中存在着乙酸正丁酯.某化学课外兴趣小组欲以乙酸和正丁醇为原料合成乙酸正丁酯.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 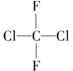 和 和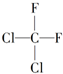 是两种不同的物质 是两种不同的物质 | |
| B. | 聚氯乙烯的单体为CH2═CHCl | |
| C. | 乙烷和乙烯均能使酸性KMnO4溶液褪色 | |
| D. | 1 mol乙酸与足量乙醇在浓硫酸催化下加热,可生成1 mol乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 200ml 2mol/L Mg Cl2溶液 | B. | 1000 ml 2.5 mol/LNaCl | ||
| C. | 300 ml 5 mol/L K Cl 溶液 | D. | 250 ml 1 mol/L AlCl3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
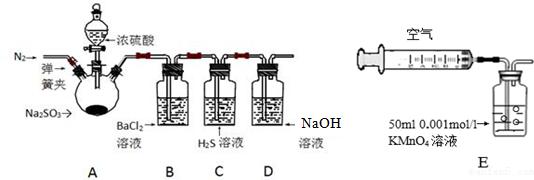
| 实验步骤 | 实验操作 | 预期现象与结论 |
| 1 | 取少量溶液于试管中,滴入几滴酚酞 | 溶液变红 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子组成符合CnH2n-2通式的链烃一定是炔烃 | |
| B. | 炔烃既易发生加成反应,又易发生取代反应 | |
| C. | 炔烃既能使溴水褪色,也能使酸性高锰酸钾溶液褪色 | |
| D. | 炔烃分子里所有的碳原子都在同一条直线上 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相对分子质量相同、结构不同的化合物一定互为同分异构体 | |
| B. | 结构对称的烷烃,其一氯代物必定只有一种 | |
| C. | 互为同分异构体的化合物不可能具有相同的结构 | |
| D. | 通式为CnH2n且碳原子数不同的有机物一定互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 在一恒温恒容密闭容器中,某化学反应2A(g)?B(g)+C(g)在三种不同条件下进行,其中实验Ⅰ、Ⅱ在800℃,实验Ⅲ在820℃,B、C的起始浓度都为0,反应物A的浓度(mol•L-1)随时间(min)变化如图所示.
在一恒温恒容密闭容器中,某化学反应2A(g)?B(g)+C(g)在三种不同条件下进行,其中实验Ⅰ、Ⅱ在800℃,实验Ⅲ在820℃,B、C的起始浓度都为0,反应物A的浓度(mol•L-1)随时间(min)变化如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com