
| A. | 金属钠与固态水分别受热熔化 | B. | 氯化铵与苯分别受热变为气体 | ||
| C. | 氯化钠与氯化氢分别溶解在水中 | D. | 碘与干冰分别受热变为气体 |
分析 根据晶体类型判断,相同类型的晶体,克服的相互作用力相同;离子晶体克服的是离子键,分子晶体的是分子间作用力,原子晶体克服的是共价键,金属晶体克服的是金属键,以此解答该题.
解答 解:A、金属钠为金属晶体,融化时破坏金属键,固态水为分子晶体,受热熔化时破坏分子间作用力,所以克服的粒子间的相互作用属不同种类型,故A不选;
B、氯化铵为离子晶体,加热分解,克服离子键,苯受热变为气体,只克服分子间作用力,故B不选;
C、氯化钠与氯化氢分别分别属于离子化合物和共价化合物,溶解在水中分别克服离子键和共价键,故C不选;
D.碘与干冰都是分子晶体,分别受热变为气体,都克服分子间作用力,故D选;
故选D.
点评 本题考查晶体类型与化学键,为高频考点,注意此类题的解题方法是:先判断晶体类型,再判断微粒间的作用力,易错点为A,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | c(OH-)<c(Cu2+)<c(H+)<c(SO42-) | B. | c(OH-)<c(H+)<c(SO42-)<c(Cu2+) | ||
| C. | c(OH-)<c(H+)<c(SO42-)=c(Cu2+) | D. | c(OH-)<c(H+)<c(Cu2+)<c(SO42-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
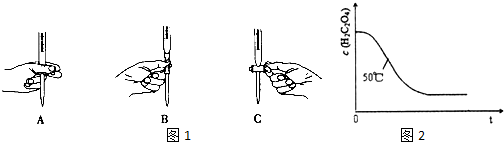
| 实验编号 | 温度(℃) | 催化剂 用量(g) | 酸性高锰酸钾溶液 | 实验目的 a.实验1和2探究探究温度不同对反应速率的影响; b.实验1和3探究反应物浓度对该反应速率的影响; c.实验1和4探究催化剂对该反应速率的影响. | |
| 体积 (mL) | 浓度 (mol•L-1) | ||||
| 1 | 25 | 0.5 | 4 | 0.1000 | |
| 2 | 50 | 0.5 | 4 | 0.1000 | |
| 3 | 25 | 0.5 | 4 | 0.0100 | |
| 4 | 25 | 0 | 4 | 0.1000 | |
| 实验编号 | 溶液褪色所需时间(min) | ||
| 第1次 | 第2次 | 第3次 | |
| 1 | 14.0 | 13.0 | 11.0 |
| 3 | 6.5 | 6.7 | 6.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AlCl3过量 | |
| B. | AlCl3的量恰好与氢氧化钠完全反应 | |
| C. | 两种碱均过量 | |
| D. | AlCl3的量恰好与氨水完全反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解熔融的氯化钠可制取金属钠,电解熔融的氧化铝可制取金属铝 | |
| B. | 电解精炼铜时,同一时间内阳极溶解铜的质量比阴极析出铜的质量小 | |
| C. | 在镀件上电镀锌,用锌作阳极,镀件作阴极 | |
| D. | 电解法精炼粗铜,用纯铜作阳极,粗铜阴极,CuSO4溶液为电解液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | b-a-4 | B. | b-a-8 | C. | b+a+8 | D. | b-a-12 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

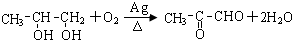 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯和苯都能使溴水褪色,褪色的原因相同 | |
| B. | 1866年凯库勒提出了苯的单、双键交替的正六边形平面结构,解释了苯的部分性质,但它不能解释的事实是邻二溴苯只有一种 | |
| C. | 光导纤维、棉花、油脂、ABS树脂都是由高分子化合物组成的物质 | |
| D. | 乙酸乙酯中的少量乙酸可用NaOH溶液除去 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com