
【题目】由两种金属组成的合金10g投入足量的稀硫酸中,反应完全后得到氢气11.2L(标准状况下),此合金可能是 ( )
A.镁铝合金B.镁铁合金C.铝铁合金D.镁锌合金
【答案】AC
【解析】
假设金属都为+2价,根据M=![]() 计算金属混合物的平衡相对原子质量,利用平均值法判断。
计算金属混合物的平衡相对原子质量,利用平均值法判断。
标准状况下11.2L氢气的物质的量为![]() =0.5mol,
=0.5mol,
假设金属都为+2价,根据电子转移守恒可知,金属的物质的量为0.5mol,则金属混合物的平均相对原子质量为20,
A.Mg的相对原子质量为24,当Al的化合价为+2价时,可看成其相对原子质量为23×27=18,金属混合物的平均相对原子质量为20,介于二者之间,故A正确;
B.Mg的相对原子质量为24,Fe的相对原子质量为56,二者平均相对原子质量介于24~56之间,故B错误;
C.当Al的化合价为+2价时,可看成其相对原子质量为23×27=18,Fe的相对原子质量为56,平均值可能为20,故C正确;
D.Mg的相对原子质量为24,Zn的相对原子质量为65,二者平均相对原子质量介于24~65之间,大于20,故D错误;
故答案选AC。


 学业测评一课一测系列答案
学业测评一课一测系列答案科目:高中化学 来源: 题型:
【题目】电化学气敏传感器可用于监测环境中![]() 的含量,其工作原理如图所示,
的含量,其工作原理如图所示,![]() 被氧气化为
被氧气化为![]() ,下列说法错误的是
,下列说法错误的是

A. 溶液中![]() 向电极b移动
向电极b移动
B. 氨气在电极a上发生氧化反应
C. 反应消耗的![]() 与
与![]() 的物质的量之比为4:5
的物质的量之比为4:5
D. 正极的电极反应式为:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式中,正确的是
A.已知:![]()
![]() ,则1mol氢气与1mol氟气反应生成2mol液态氟化氢放出的热量小于
,则1mol氢气与1mol氟气反应生成2mol液态氟化氢放出的热量小于![]() kJ
kJ
B.![]() 、30MPa下,将
、30MPa下,将![]() mol
mol![]() 和
和![]() mol
mol![]() 置于密闭容器中充分反应生成
置于密闭容器中充分反应生成![]() 放热
放热![]()
![]() 其热化学方程式为:
其热化学方程式为:![]()
![]()
C.![]()
![]() ,则
,则![]()
D.在101kPa时,2g![]() 完全燃烧生成液态水,放出
完全燃烧生成液态水,放出![]() kJ热量,氢气燃烧的热化学方程式表示为
kJ热量,氢气燃烧的热化学方程式表示为![]()
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜和镁的合金4.6 g完全溶于浓硝酸,若反应中硝酸被还原只产生4 480 mL NO2气体和336 mL的N2O4气体(气体的体积已折算到标准状况),在反应后的溶液中,加入足量的氢氧化钠溶液,生成沉淀的质量为 ( )
A.9.02 gB.8.51 gC.8.26 gD.7.04 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将2.1g 由CO 和H2 组成的混合气体,在足量的O2 充分燃烧后,立即通入足量的Na2O2 固体中,固体的质量增加
A.2.1gB.3.6gC.4.2gD.7.2g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乳酸亚铁晶体{[CH3CH(OH)COO]2Fe·3H2O}(相对分子质量:288)可由乳酸与FeCO3反应制得,它易溶于水,几乎不溶于乙醇,受热易分解,是一种很好的补铁剂。
乳酸亚铁晶体纯度的测量:用K2Cr2O7滴定法测定样品中Fe2+的含量计算样品纯度,称取6.00g样品配制成250.00mL溶液。取25.00mL用0.0167mol·L-1的K2Cr2O7标准溶液滴定至终点,消耗标准液20.00mL。则产品中乳酸亚铁晶体的纯度为___(以质量分数表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属材料、无机非金属材料、有机高分子材料是人类使用的三大类基础材料,它们以各自的特点满足着人类多方面的需要。
(1)金属材料中,有一类贮氢合金能够结合氢气形成金属化合物,并在一定条件下分解释放出氢气,该贮运原理属于_______变化,钢铁是制造轮船的主要金属材料,船身外通常装上一定数目比铁更活泼的金属块以防止腐蚀,该金属块可以选择_______(选填“铜块”、“锌块”、“铅块”);
(2)无机非金属材料中,用于电子工业的高纯碳酸钙、高纯氧化钙生产流程如下:

请回答下列问题:
①硝酸钙与碳酸铵在溶液中反应,其基本反应类型为_______;
②实验室常采用_______操作进行沉淀分离;
③生产高纯碳酸钙时,选择“220℃恒温干燥”而不选择“灼烧”的原因是_______;
④高纯氧化钙生产过程中,“干燥”的主要目的是为了防止______(用化学方程式表示);
(3)有机高分子材料“玉米塑料”,因其可降解被广泛用来替代一次性泡沫塑料,“玉米塑料”的使用可减少_______污染,20世纪30年代,尼龙因其抽成细丝极像蚕丝而被推向世界,生活中可采用______方法区分尼龙和蚕丝。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在一个2 L的密闭容器中,加入4 mol A和2 mol B进行如下反应:
3A(g)+2B(g)![]() 4C(s)+2D(g),反应一段时间后达到平衡,测得生成1.6 mol C,则下列说法正确的是
4C(s)+2D(g),反应一段时间后达到平衡,测得生成1.6 mol C,则下列说法正确的是
A.该反应的化学平衡常数表达式是K=![]()
B.此时,B的平衡转化率是40%
C.增大该体系的压强,化学平衡常数增大
D.增加C,平衡时混合气体密度增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某铅酸蓄电池的工作原理如图所示,其总反应式为![]() 。下列判断不正确的是
。下列判断不正确的是
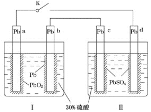
A.闭合K时,d电极的反应式为![]()
B.当电路中转移![]() 电子时,Ⅰ中消耗的
电子时,Ⅰ中消耗的![]() 为
为![]()
C.闭合K时,Ⅱ中![]() 向c电极迁移
向c电极迁移
D.闭合K一段时间后,Ⅱ可单独作为原电池,d电极为正极
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com