
| A、①③ | B、②④ |
| C、①③④ | D、①②③④ |


科目:高中化学 来源: 题型:

| 140℃ |
| 名称 | 相分子质量 | 密度 g/mL | 熔点 ℃ | 沸点 ℃ | 溶解度:g/100mL溶剂 | ||
| 水 | 醇 | 醚 | |||||
| 浓H2SO4 | 98.00 | 1.84 | 10.35 | 340 | |||
| 乙醚 | 74.00 | 0.71 | -89.12 | 34.5 | 能溶 | 混溶 | 混溶 |
| 乙醇 | 46.00 | 0.780 | -114.5 | 78.4 | ∞ | ∞ | ∞ |

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
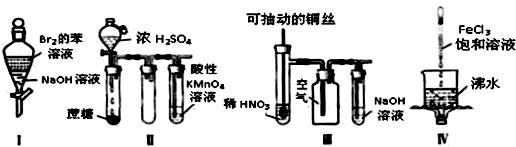
| A、Ⅰ:振荡后静置,上层溶液颜色保持不变 |
| B、Ⅱ:酸性KMnO4溶液中出现气泡,且颜色逐渐褪去 |
| C、Ⅲ:微热稀HNO3片刻,溶液中有气泡产生,广口瓶内始终保持无色 |
| D、Ⅳ:继续煮沸溶液一定能得到氢氧化铁胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、若在移液过程中,溶液溅出容量瓶,则应重新配制溶液 |
| B、将5.85gNaCl固体溶于1 L水中可配成0.1 mol?L-1的NaCl溶液 |
| C、固体直接转移到容量瓶中,并加水稀释到刻度线 |
| D、称量时,将固体NaCl直接放在天平左盘上 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温时的水溶性:Na2CO3<NaHCO3 |
| B、等物质的量时与足量酸反应产生CO2的量:Na2CO3>NaHCO3 |
| C、与等浓度稀盐酸反应的快慢:Na2CO3<NaHCO3 |
| D、同质量时消耗盐酸的量:Na2CO3<NaHCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、电流计指针偏转时,说明发生了氧化还原反应 |
| B、苹果汁中无电解质 |
| C、两个电极的材料可以相同 |
| D、水果电池工作时氧化反应和还原反应在同一处进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图是一个乙醇燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,请回答下列问题:
如图是一个乙醇燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、6.4 | B、4.8 |
| C、3.2 | D、2.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com