
��9�֣�������������Ҫ������������ԭ��������ˮ��Һ�ֳ�Ϊ˫��ˮ����������
����ɱ����Ư�ȡ�ij��ѧ��ȤС��ȡһ�����Ĺ���������Һ����ȷ�ⶨ������
��ĺ���������д���пհף�
��1��ȡ10.00 mL�ܶ�Ϊ��g/mL�Ĺ���������Һϡ����250mL����ȡϡ�ͺ�Ĺ�����
����Һ25.00mL����ƿ�У�����ϡ�����ữ��������ˮϡ�ͣ�������������
��2���ø�����ر���Һ�ζ������������䷴Ӧ�����ӷ���ʽΪ ��
��3���ζ�ʱ����������ر���Һע�� �����ʽ����ʽ�����ζ���
�У��ζ������յ�������� ��
��4���ظ��ζ����Σ�ƽ������c mol/L KMnO4����ҺV mL����ԭ����������Һ��
�����������������Ϊ ��
��5�����ζ�ǰ�ζ��ܼ����������ݣ��ζ���������ʧ����ⶨ��� ���ƫ�ߡ���ƫ�͡����䡱����
��9�֣�
��2��2MnO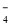 ��5H2O2��6H+��2Mn2+��8H2O��5O2����2�֣�
��5H2O2��6H+��2Mn2+��8H2O��5O2����2�֣�
��3����ʽ��1�֣�
�������һ�θ��������Һ����Һ���Ϻ�ɫ����30���ڲ���ɫ��2�֣�
��4��0.085cV/�� [��(8.5cV/��)%] ��2�֣�
��5��ƫ�ߣ�2�֣�
��������
�����������2�����Ը��������������ⷢ��������ԭ��Ӧ���������ⱻ����Ϊ������������ر���ԭΪ�����ӣ����ӷ���ʽΪ2MnO4-��5H2O2��6H+��2Mn2+��8H2O��5O2����
��3��������ص�������ǿ������Ӧ����ʽ�ζ���ʢ�ţ�������ر�������ɫ��Һ�����Եζ��յ�ʱ�������ǵ������һ�θ��������Һ����Һ���Ϻ�ɫ����30���ڲ���ɫ��
��4���������ӷ���ʽ��֪25mL��Һ�й�����������ʵ�����5/2cV��10-3mol����ԭ��Һ�й��������������10��5/2cV��10-3mol��34g/mol=85cV��10-2g��ԭ����������Һ��������10��g�����Թ������������������85cV��10-2g/10��g=0.085cV/�ѣ�
��5�����ζ�ǰ�ζ��ܼ����������ݣ��ζ���������ʧ����ζ�ǰ����ֵƫС�����Լ�����������Һ�����ƫ�ⶨ���ƫ�ߡ�
���㣺����ζ�ʵ��ķ��������㡢������


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���㽭ʡ���������ѧУ�߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����ͬ��Ũ�Ⱦ�Ϊ0.1mol/L��NaOH��Һ����ˮ���ֱ��ˮϡ��m����n������Һ��pH�����9����m��n�Ĺ�ϵΪ
A��4m��n B��m��n C��m<n D��m>n
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���㽭̨����ѧ�߶���ѧ�ڵ�һ��ͳ����ѧ�Ծ��������棩 ���ͣ�ѡ����
������,�ֱ��Ŀ���״��ͬ,����Ϊ7 g������ͬʱͶ������������Һ��,������������������
A��200 mL 2 mol��L��1HCl B��100 mL 2 mol��L��1H2SO4
C��100 mL 3 mol��L��1HNO3 D��50 mL 18.4 mol��L��1H2SO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����۳���ص�һ���и߶��ϵ�һ�ο��Ի�ѧ��B���Ծ��������棩 ���ͣ�ѡ����
��֪���и��鷴Ӧ�ķ�Ӧ�P�¶ȣ���Ӧ��ʼʱ���ų�H2�����������ǣ����е����ʾ�Ϊ��Ӧ�
��� | ��������С����״��ͬ�ķ�ĩ�����ʵ��� | ���Ũ�ȼ���� | ��Ӧ�¶�/�� |
A | Mg 0.1 mol | 3 mol/L������10 mL | 60 |
B | Mg 0.1 mol | 3 mol/L������10 mL | 30 |
C | Fe 0.1 mol | 3 mol/L������10 mL | 60 |
D | Mg 0.1 mol | 3 mol/L������10 mL | 60 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����۳���ص�һ���и߶��ϵ�һ�ο��Ի�ѧ��B���Ծ��������棩 ���ͣ�ѡ����
��֪H2(g)��Br2(l)��2HBr(g) ��H����72kJ��mol��1������1mol Һ���Br2(g)��Ҫ���յ�����Ϊ30kJ����������������±���
| H2(g) | Br2(g) | HBr(g) |
1mol�����еĻ�ѧ������ʱ��Ҫ���յ�����/kJ | 436 | a | 369 |
�����aΪ
A��404 B��260 C��230 D��200
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����۳���ص�һ���и߶��ϵ�һ�ο��Ի�ѧ��A���Ծ��������棩 ���ͣ�ѡ����
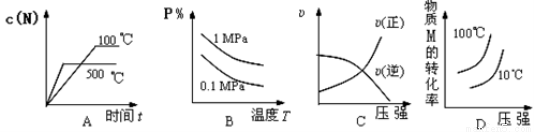
���ڿ��淴Ӧ��2M(g)+N(g) 2P(g) ��H��0�����и�ͼ����ȷ����( )
2P(g) ��H��0�����и�ͼ����ȷ����( )
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����۳���ص�һ���и߶��ϵ�һ�ο��Ի�ѧ��A���Ծ��������棩 ���ͣ�ѡ����
һ���¶�����һ�ݻ�������ܱ������з������淴Ӧ2X(g) Y(g)��Z(s)�����²���˵���÷�Ӧ�ﵽ��ѧƽ��״̬����
Y(g)��Z(s)�����²���˵���÷�Ӧ�ﵽ��ѧƽ��״̬����
A��2v��(X)��v��(Y) B����λʱ��������1 mol Y��ͬʱ����2 mol X
C�����������ܶȲ��ٱ仯 D����Ӧ������Y��������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����۳���ص�һ���и�һ�ϵ�һ�ο��Ի�ѧ��B���Ծ��������棩 ���ͣ�ѡ����
��һ���ƿ����Ϊ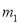 ����ƿ�������������Ϊ
����ƿ�������������Ϊ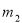 ������ͬ״���£�����Ϊ����ij����Aʱ��������Ϊ
������ͬ״���£�����Ϊ����ij����Aʱ��������Ϊ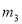 ����A����Է��������ǣ� ��
����A����Է��������ǣ� ��
A�� ��29 B��
��29 B��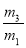 ��29 C��
��29 C��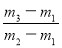 ��29 D��
��29 D��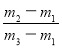 ��29
��29
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����֣���и�һ��10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��ͼ��A��ͨ���������ر�B��ʱ,C����ɫ�����ޱ仯����B��ʱ��C����ɫ������ɫ���� ���������ж���ȷ���� �� ��

A�� D�в�������Ũ���� B�� ͨ�����������ˮ����.
C�� D�п�����ˮ D�� D�п����DZ���ʳ��ˮ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com