
分析 依据化学平衡三段式列式计算,恒温恒压气体体积之比等于气体物质的量之比,设起始量氮气和氢气为1,3,氮气反应的物质的量为x
N2+3H2?2NH3
起始量(mol) 1 3 0
变化量(mol) x 3x 2x
平衡量(mol) 1-x 3-3x 2x
混合气体中NH3占25%,则$\frac{2x}{4-2x}$=25%
x=0.4
(1)转化率=$\frac{消耗量}{起始量}$×100%
(2)恒温恒压气体体积之比等于气体物质的量之比;
(3)反应前后气体质量不变,平衡时混合气体的相对分子质量=$\frac{总质量}{总物质的量}$.
解答 解:恒温恒压气体体积之比等于气体物质的量之比,设起始量氮气和氢气为1,3,氮气反应的物质的量为x,
N2+3H2?2NH3
起始量(mol) 1 3 0
变化量(mol) x 3x 2x
平衡量(mol) 1-x 3-3x 2x
混合气体中NH3占25%,则$\frac{2x}{4-2x}$=25%
x=0.4
(1)N2的转化率=$\frac{消耗量}{起始量}$×100%=$\frac{0.4mol}{1mol}$×100%=40%,
故答案为:40%;
(2)恒温恒压气体体积之比等于气体物质的量之比,反应前后体积之比=(1+3):(1-x+3-3x+2x)=4:(4-2×0.4)=5:4,
故答案为:5:4;
(3)反应前后气体质量不变,平衡时混合气体的相对分子质量=$\frac{总质量}{总物质的量}$=$\frac{1mol×28g/mol+3mol×2g/mol}{(4-2×0.4)mol}$=10.625,
故答案为:10.625.
点评 本题考查了化学平衡三段式计算分析应用,主要是转化率,混合气体的相对分子质量计算应用,气体体积之比等于气体物质的量之比,题目难度中等.


科目:高中化学 来源: 题型:解答题
| 实验 步骤 | 实验操作 | 预期现象及结论 (步骤1只写现象) |
| 1 | 在A、B两支洁净的试管中各加入1mL 2%的AgNO3溶液,然后边振荡试管边逐滴滴入2%稀氨水, 至沉淀恰好溶解,此时制得pH均约为8的银氨溶液. | 先生成白色沉淀,后沉淀溶解. |
| 2 | 往A、B试管加入3滴乙醛,然后在A试管中加1滴NaOH溶液;振荡后将两支试管放在热水浴中温热. | 若A试管比B试管出现的银镜时间短、光亮,则则溶液pH大,反应速率快; 若A试管比B试管出现的银镜时间长,则则溶液pH大,反应速率慢. |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
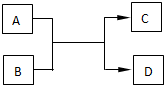 学习了元素周期表,可以帮助我们进一步丰富不同元素间的相互转化关系.已知A、B、C、D都处于短周期,A、D为单质,B、C是化合物.
学习了元素周期表,可以帮助我们进一步丰富不同元素间的相互转化关系.已知A、B、C、D都处于短周期,A、D为单质,B、C是化合物.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丁硫醇、甲硫醇与乙硫醇互为同系物 | |
| B. | 沸点不同的丁硫醇有四种 | |
| C. | 丁硫醇在空气中燃烧生成二氧化碳、二氧化硫和水 | |
| D. | 在水溶液中,乙硫醇比乙醇更难电离出H+离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
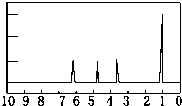 有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取.纯净的A为无色黏稠液体,易溶于水.为研究A的组成与结构,进行了如下实验:
有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取.纯净的A为无色黏稠液体,易溶于水.为研究A的组成与结构,进行了如下实验: .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠的金属活泼性大于铜,在溶液中钠可以置换出铜 | |
| B. | 在稀硫酸中加入铜粉,铜粉不溶解,再加入KNO3固体,铜粉仍不溶解 | |
| C. | 在KI溶液中加入NaNO3,没有明显现象,加入盐酸,即有I2生成 | |
| D. | 纯锌与稀硫酸反应产生氢气的速率较,加入少量CuSO4固体,速率不改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用系统命名:CH3CH(C2H5)CH2CH2CH3 2-乙基戊烷 | |
| B. | 2-甲基戊烷和2,2-二甲基丁烷互为同分异构体,C2H6和C3H8一定互为同系物 | |
| C. | 将(NH4)2SO4、CuSO4溶液分别加入蛋白质溶液,都出现沉淀,表明二者均可使蛋白质变性 | |
| D. | 糖类、油脂和蛋白质均可发生水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | A | B | C | D |
| n(CO2)(mol) | 1 | 1.5 | 2 | 3 |
| n(沉淀)(mol) | 0.5 | 1 | 1.5 | 1 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com