
| 1.0 MPa | 2.0 MPa | 3.0 MPa | |
| 800�� | a | b | 83% |
| 900�� | c | 75% | d |
| 1000�� | 54% | e | f |
| A�� | 4�� | B�� | 3�� | C�� | 2�� | D�� | 1�� |
���� ��X��g��+Y��g��?Z ��s��+2W��g������Ӧǰ��������������䣬����ͬ�¶��£�����Ӱ��ƽ���ƶ�����a=b=83%��c=d=75%��e=f=54%��
��900��ʱX��g��+Y��g��?Z ��s��+2W��g����
��ʼ n n 0
ת�� x x 2x
ƽ�� n-x n-x 2x
��$\frac{2x}{2n-2x+2x}$=75%�����x=$\frac{3}{4}$n��
���ɱ������ݿ�֪���¶�Խ�ߣ�ƽ��ʱW���������ԽС��
�ܷ��ȷ�Ӧ���¶�Խ�ߣ�KԽС��
��� �⣺��X��g��+Y��g��?Z ��s��+2W��g������Ӧǰ��������������䣬����ͬ�¶��£�����Ӱ��ƽ���ƶ�����a=b=83%��c=d=75%��e=f=54%����a��c��f������ȷ��
��900��ʱX��g��+Y��g��?Z ��s��+2W��g����
��ʼ n n 0
ת�� x x 2x
ƽ�� n-x n-x 2x
��$\frac{2x}{2n-2x+2x}$=75%�����x=$\frac{3}{4}$n����900�桢2.0MPaʱ��X��ת����Ϊ$\frac{\frac{3}{4}n}{n}$��100%=75%������ȷ��
���ɱ������ݿ�֪���¶�Խ�ߣ�ƽ��ʱW���������ԽС���������¶ȣ�ƽ�������ƶ�������ӦΪ���ȷ�Ӧ������H��0������ȷ��
�ܷ��ȷ�Ӧ���¶�Խ�ߣ�KԽС��ƽ�ⳣ��K��1000�棩��K��800�棩���ʴ���
��ѡB��
���� ���⿼�黯ѧƽ��ļ��㣬Ϊ��Ƶ���㣬����ƽ�����η���ת���ʵļ��㼰ƽ���ƶ���Ӱ��Ϊ���Ĺؼ������ط�������������Ŀ��飬ע��ѹǿ�ı�ʱ��ƽ�ⲻ�ƶ�����Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2 c1��c2 | B�� | c1��c2 | C�� | c1=c2 | D�� | 2 c1=c2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2Q2=Q1=92.4 | B�� | Q2��Q1��92.4 | C�� | Q1=Q2=92.4 | D�� | Q1��Q2��92.4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
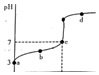 R֪ij�¶ȵ���ƽ�ⳣ��ΪK�����¶�����20mL 0.1mol/L CH3COOH��Һ����μ���0•1mol/L NaOH��Һ����pH�仯������ͼ��ʾ�������¶ȱ仯��������˵������ȷ���ǣ�������
R֪ij�¶ȵ���ƽ�ⳣ��ΪK�����¶�����20mL 0.1mol/L CH3COOH��Һ����μ���0•1mol/L NaOH��Һ����pH�仯������ͼ��ʾ�������¶ȱ仯��������˵������ȷ���ǣ�������| A�� | a���ʾ��Һ��c��CH3COO-��-��Ϊ10-3 mol/L | |
| B�� | b���ʾ����Һ��c��Na+����c��CH3COO-�� | |
| C�� | c���ʾCH3COOH��NaOHǡ�÷�Ӧ��ȫ | |
| D�� | d���ʾ����Һ��$\frac{c��C{H}_{3}CO{O}^{-}��}{c��C{H}_{3}COOH��}$����K |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ��Ӧʱ��/min | n��A��/mol | n��B��/mol |
| 0 | 1.00 | 1.20 |
| 10 | 0.50 | |
| 30 | 0.20 |
| A�� | ǰ10min�ڷ�Ӧ��ƽ������Ϊv��C��=0.050mol•L-1•min-1 | |
| B�� | ���������������䣬��ʼʱ�������г���0.50molA�����0.60molB���壬����ƽ��ʱ��n��C����0.25mol | |
| C�� | ���ܱ�����������䣬�����������䣬�ڴﵽƽ��������С�����������ƽ��һֱ�������ƶ� | |
| D�� | �¶�ΪT2��ʱ��T1��T2����������Ӧƽ�ⳣ��Ϊ20��������ӦΪ���ȷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��״���£�22.4LH2O����ԭ�Ӹ�������3NA | |
| B�� | 100ml18.4mol/L����������Cu��Ӧ������SO2�ķ�����Ϊ0.92NA | |
| C�� | t��ʱ��MgCO3��Ksp=4��10-6������Һ�к�Mg2+��ĿΪ2��10-3NA | |
| D�� | 100g��������Ϊ34.2%�����Ƿ���ˮ��Һ�к�Hԭ����Ϊ2.2NA |
�鿴�𰸺ͽ���>>
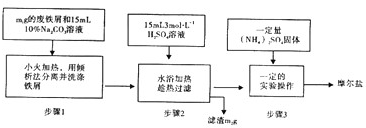
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2C2H6��g��+7O2 ��g��=4CO2 ��g��+6H2O��l������H=-1190KJ/mol | |
| B�� | C2H6��g��+$\frac{7}{2}$O2 ��g��=2CO2 ��g��+3H2O��g������H=-1190KJ/mol | |
| C�� | 298k��101kPaʱ��30g����������ȫȼ������CO2�����Һ̬ˮ���ų�1190kJ���� | |
| D�� | �÷�Ӧ�У���Ӧ�������е�������С�������������е������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com