
| 3 |
| 2 |
| 3 |
| 2 |
| 3 |
| 2 |
| 728KJ |
| 2 |
| 345.8kJ |
| 364KJ |


科目:高中化学 来源: 题型:
| A、1项 | B、2项 | C、3项 | D、4项 |
查看答案和解析>>
科目:高中化学 来源: 题型:
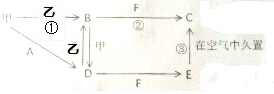
查看答案和解析>>
科目:高中化学 来源: 题型:
| 离子符号 | K+ | SO42- | Cl- |
| 物质的量浓度(mol?L-1) | 9.0 | 4.0 | 9.0 |
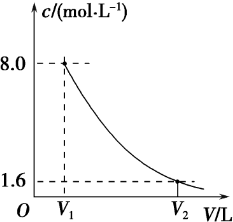
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、某吸热反应能自发进行,则该反应的△S>0 |
| B、SO2使酸性KMnO4溶液褪色,因此SO2具有漂白性 |
| C、在物质分离的方法中,蒸馏、萃取、重结晶都与物质的溶解度有关 |
| D、用浓硫酸代替稀硫酸与铁反应能加快生成H2的速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、0.5mol雄黄(As4S4,结构如图)含有NA个S-S键 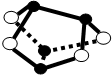 |
| B、1mol/L(NH4)2SO4溶液中,含SO42-NA个,NH4+少于2NA个 |
| C、23g钠与一定量的氧气作用,若两者均无剩余,转移NA个电子 |
| D、将含0.1 mol FeCl3的溶液滴加到沸水中完全水解可生成0.1 NA个Fe(OH)3胶粒 |
查看答案和解析>>
科目:高中化学 来源: 题型:
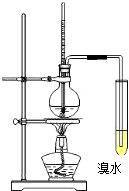 实验室以浓硫酸和酒精为原料制取乙烯并进行乙烯性质实验的装置如图所示.
实验室以浓硫酸和酒精为原料制取乙烯并进行乙烯性质实验的装置如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度/℃ | 1538 | 1760 | 2404 |
| 平衡常数K | 0.86×10-4 | 2.6×10-4 | 64×10-4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③⑤⑦ | B、②④⑤ |
| C、①③④ | D、①②③④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com