
| A�����ʵ���������Ϊ������100% |
| B����ˮ�����ʵ���Ũ��Ϊ1000a/(35V)mol��L��1 |
| C����Һ��c(OH��)��1000b/V mol��L��1��c(H��) |
| D��������Һ���ټ���V mLˮ��������Һ��������������0.5�� |
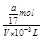 =
=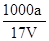 mol/L����D��ȷ��
mol/L����D��ȷ��

 ÿ��10���ӿ�����������������ϵ�д�
ÿ��10���ӿ�����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A��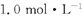 �İ�ˮ�� �İ�ˮ��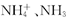 �� ��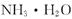 ������Ϊ ������Ϊ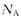 |
| B��1 mol Na2O2������H2O��ַ�Ӧ��ת�Ƶĵ�����Ϊ2NA |
| C��0.1 mol Cu������Ũ���ᷴӦ����SO2�����ԼΪ4.48 L |
| D�����³�ѹ�£�21g������27 g������������ԭ������Ϊ3NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����״���£�5.6 L���Ȼ�̼���еķ�����Ϊ0.25NA |
| B����״���£�14 g�������еĺ��������Ϊ5NA |
| C����״���£�22.4 L����ȵ������������Ļ�������к��еķ���������ΪNA |
| D���ڱ�״���£�18gH2O�����еĵ���������10 NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��V/4 mL | B��V/3 mL | C��V/5 mL | D�����ж� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����³�ѹ�£�2��2g14CD4���������� |
| B�����³�ѹ�£�46g�����������������������������������ԭ������ |
| C����״���£�11��2LH2O���������� |
| D��1��0L 1mol/L��ˮ�У�NH3��H2O�ķ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��6.2 g Na2O��7.8 g Na2O2�������������� |
| B����⾫��ͭʱ�����ܽ�������������ͭ������ |
| C��11.2 L N2��14 g CO���������е�ԭ���� |
| D��20 g��ˮ(D2O)��17 g NH3�����еĵ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���٢� | B���٢ܢ� | C���ڢ� | D���ڢۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�������£�pH=1�Ĵ�����Һ�У�������ӵ���Ŀһ������0.1NA |
| B��22.4LCH4��CH3Cl�Ļ���������еķ�����ĿΪNA |
| C��5.6 g������0.1mol�����г��ȼ�գ�ʧȥ�ĵ�����Ϊ0.3NA |
| D��1mol������������й��õ��Ӷ���Ϊ3NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 ϡ����
ϡ����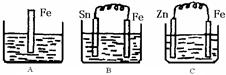
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com