
科目:高中化学 来源: 题型:选择题
| A. | 将溶液稀释到原体积的10倍 | B. | 加入适量的NH4Cl固体 | ||
| C. | 加入等体积0.2mol•L-1NaOH溶液 | D. | 提高溶液的温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Ba2+、NO3-、Cl-、 | B. | H+、Fe2+、ClO-、SO42- | ||
| C. | K+、Fe3+、Cl-、SCN- | D. | NH4+、Al3+、SiO32-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
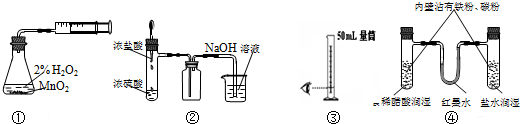
| A. | 装置①制取并收集纯净的氧气 | B. | 装置②制取并吸收HCl | ||
| C. | 装置③量取8.5mL的稀硫酸 | D. | 装置④模拟铁的腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
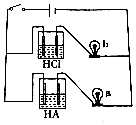
| A. | HA属于弱酸 | |
| B. | pH=1的HA溶液中由水电离出的c(H+)=10-13•L-1 | |
| C. | 等体积、等pH的HA和HCl溶液分别和NaOH溶液反应,HA消耗的NaOH较多 | |
| D. | 等体积的上述两种酸溶液分别和NaOH溶液反应,HA消耗的NaOH较少 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| W | |||
| Y | Z |
| A. | X能分别与Y、W形成化合物,且其所含化学键类型完全相同 | |
| B. | W有多种同素异形体,且均具有高熔点、高沸点的性质 | |
| C. | X的离子半径一定小于Y同族的短周期元素的离子半径 | |
| D. | Y、Z与X的常见稳定液态氧化物反应的剧烈程度Y大于Z |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
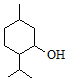
| A. | 薄荷醇分子式为C10H20O,它是环己醇的同系物 | |
| B. | 薄荷醇的分子中至少有12个原子处于同一平面上 | |
| C. | 薄荷醇在Cu或Ag做催化剂、加热条件下能被O2氧化为醛 | |
| D. | 在一定条件下,薄荷醇能发生取代反应、消去反应和聚合反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com