
下列试管实验的方案中,一定能达到实验目的是
A.制备乙酸丁酯:加入正丁醇和乙酸,再滴加几滴浓硫酸,振荡,水浴加热
B.检验甲基橙试液中是否混有微量酚酞:按图所示上升纸上层析法实验

C.检验醛基:加入CuSO4溶液和NaOH溶液各1mL,振荡,加入乙醛溶液,煮沸
D.比较苯酚、乙酸、碳酸的酸性:乙酸和纯碱反应产生的气体通入苯酚钠溶液中
【答案】B
【解析】
试题分析:A、制备乙酸丁酯:先加入正丁醇,然后逐滴加入几滴浓硫酸,震荡冷却后在加入乙酸,A不正确;B、甲基橙与酚酞是两种常见的酸碱指示剂,它们在水中和有机溶剂中的溶解度不同,酚酞易溶于酒精而不溶于水;甲基橙易溶于水。当有机溶剂沿滤纸流经混合物的点样时,甲基橙和酚酞会以不同的速度在滤纸上移动,酚酞的移动速度快于甲基橙,形成不同的色斑,内部的黄斑为甲基橙,外部的红色斑为酚酞,从而达到分离的目的,B正确;C、在制备氢氧化铜悬浊液时氢氧化钠应该是过量的,所以选项C不正确;D、乙酸易挥发,生成的CO2气体中含有乙酸,所以在通入到苯酚钠溶液中之前需要除去CO2中的乙酸,D不正确,答案选B。
考点:考查实验基本操作、实验方案设计与评价等


 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:
卤素化学丰富多彩,能形成卤化物、卤素互化物、多卤化物等多种类型的化合物。
(1)基态溴原子的价电子排布式为___________。
(2)卤素互化物如IBr、ICl等与卤素单质结构相似、性质相近。则Cl2、IBr、ICl的沸点由高到低的顺序为___________。
(3)气态氟化氢中存在二聚分子(HF)2,这是由于___________。
(4)I3+属于多卤素阳离子,根据VSEPR模型推测I3+的空间构型为___________,中心原子杂化类型为___________。
(5)①HClO4、②HIO4、③H5IO6〔可写成(HO)5IO〕的酸性由强到弱的顺序为___________(填序号)。
(6)IBr和水能发生反应,生成物中有一种为三原子分子,写出该化合物的结构式__________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
A~G是几种烃的分子球棍模型(如图),据此回答下列问题:
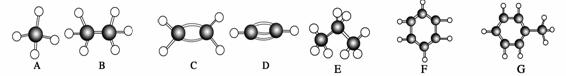
(1)能够发生加成反应的烃有(填数字)________种;
(2)常温下含氢量最高的气态烃是(填对应字母)________;
(3)一卤代物种类最多的是(填对应字母)________;
(4)A~G在充有足量氧气的密闭恒容容器中完全燃烧,150℃时测得燃烧前后的压强不变的有 ___________(填对应字母)
(5)写出实验室制取D的化学方程式 ;
查看答案和解析>>
科目:高中化学 来源: 题型:
无色的混合气体甲,可能含NO、CO2 、NH3 、H2的几种,将100ml甲气体经过下图实验的处理,结果得到酸性溶液,而几乎无气体剩余,则甲气体的组成为 ( )
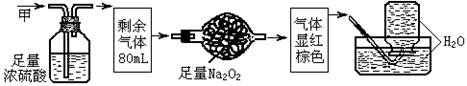
A. NH3、NO2、N2 B. NH3、NO、CO2 C. NH3、NO2、CO2 D. NO、CO2、N2
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)已知 2Na+2H2O=2NaOH+H2↑中水是氧化剂,请写出一个水做还原剂的置换反应的化学反应方程式______________________
(2)瑞典化学家舍勒将软锰矿(主要成分MnO2)与浓盐酸混合加热,在世界上首先制得了氯气,写出该反应的离子方程式_____________________________________________
⑶洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。 漂白粉是常用的消毒剂。工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为
______________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验能很好达到预期目的的是
A.向AlCl3溶液中加入NaOH溶液使铝离子恰好完全转化为Al(OH)3沉淀
B.向AgCl悬浊液中加入KI溶液,沉淀由白色转化为黄色,证明溶解性AgI<AgCl
C.向试管中的银氨溶液滴加A物质,水浴加热,若产生银镜,说明A物质是醛类
D.用湿润的pH试纸测试未知浓度盐酸的c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
用下列装置能达到有关实验目的是






① ② ③ ④
A.用①量取15.00 mL NaOH溶液
B.用②制备并收集少量NO2气体
C.用③所示的仪器配制1L 0.1000mol/LNaCl溶液
D.用④进行Fe2+的检验
查看答案和解析>>
科目:高中化学 来源: 题型:
【化学——化学与技术】(15分)
 高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺如下:
高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺如下:
已知:①2KOH + Cl2 = KCl + KClO + H2O(条件:温度较低)
②6KOH + 3Cl2 = 5KCl + KClO3 + 3H2O(条件:温度较高)
③2Fe(NO3)3 + 2KClO + 10KOH = 2K2FeO4 + 6KNO3 + 3KCl + 5H2O
回答下列问题:
(1)该生产工艺应在 (填“温度较高”或“温度较低”)的情况下进行;
(2)写出工业上制取Cl2的化学方程式 ;
(3)K2FeO4可作为新型多功能水处理剂的原因 ;
(4)配制KOH溶液时,是在每100 mL水中溶解61.6 g KOH固体(该溶液的密度为
1.47 g/mL),它的物质的量浓度为 ;
(5)在“反应液I ”中加KOH固体的目的是① ,
② ;
(6)从“反应液II ”中分离出K2FeO4后,副产品是 (写化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com