
����Ŀ������ȼ�ϵ���Ƿ�����ɫ��ѧ��������ͷ���װ�ã�
��ͼΪ���ʾ��ͼ���õ�ص缫�����һ��ϸС�IJ��ۣ����������������ǿ�������ȶ�����ش�
��1������ȼ�ϵ�ص�����ת������Ҫ��ʽ���� �� �ڵ����е�����������Ϊ����a��b��ʾ����
��2��������ӦʽΪ ��
��3���缫����Ʋ��۵�ԭ���� ��
��4���õ�ع���ʱ��H2��O2�������ⲿ��������ؿ����������ṩ���ܣ���ˣ�������ȫ�����ǹؼ�����֮һ���������һ����Ҫ�Ĵ�����ϣ�����ͷ���ԭ�����£�
��2Li+H2 ![]() 2LiH
2LiH
��LiH+H2O�TLiOH+H2��
�ٷ�Ӧ���еĻ�ԭ���� �� ��Ӧ���е��������� �� �����ѧʽ��
����֪LiH�����ܶ�Ϊ0.82g/cm3 �� �������224L����״����H2 �� �����յ�H2��������ɵ�LiH�����Ϊ ��
���ɢ����ɵ�LiH��H2O���ã��ų���H2�������ȼ�ϣ�������ת����Ϊ80%��������ͨ�����ӵ����ʵ���Ϊmol��
���𰸡�
��1����ѧ��ת��Ϊ���ܣ���a��b
��2��2H2+4OH����4e��=4H2O����H2+2OH����2e��=2H2O��
��3������缫��λ�������H2��O2���������ӿ�缫��Ӧ����
��4��Li��H2O��1148��1��32
���������⣺��1��ԭ�����Ҫ�ǽ���ѧ��ת��Ϊ���ܣ�ȼ�ϵ����ԭ��أ��ǽ���ѧ��ת��Ϊ���ܵ�װ�ã�����ʧȥ���ӣ�Ϊ������������õ��ӣ�Ϊ�����������ɸ���ͨ��������������������a��b�����Դ��ǣ���ѧ��ת��Ϊ���ܣ���a��b����2������������ʧ���Ӻ����������ӷ�Ӧ����ˮ���缫��ӦʽΪ2H2+4OH����4e��=4H2O����H2+2OH����2e��=2H2O�������Դ��ǣ�2H2+4OH����4e��=4H2O����H2+2OH����2e��=2H2O������3����Ӧ��Ӵ����Խ��Ӧ����Խ�Ʋ�������缫��λ��������������������������ӿ�缫��Ӧ���ʣ����Դ��ǣ�����缫��λ�������H2��O2���������ӿ�缫��Ӧ���ʣ���4����2Li+H2 ![]() 2LiH���÷�Ӧ���ʧ���ӷ���������Ӧ��������ǻ�ԭ����LiH+H2O=LiOH+H2�����÷�Ӧ��H2O�õ�������������������ԭ��Ӧ������H2O�������������Դ��ǣ�Li��H2O������LiH���ΪvL�����ʵ���Ϊn=
2LiH���÷�Ӧ���ʧ���ӷ���������Ӧ��������ǻ�ԭ����LiH+H2O=LiOH+H2�����÷�Ӧ��H2O�õ�������������������ԭ��Ӧ������H2O�������������Դ��ǣ�Li��H2O������LiH���ΪvL�����ʵ���Ϊn= ![]() ��mol�������ݷ�Ӧ����ʽ��2n��H2��=n��LiH������
��mol�������ݷ�Ӧ����ʽ��2n��H2��=n��LiH������ ![]() ��mol��=2��
��mol��=2�� ![]() =20mol��v=
=20mol��v= ![]() L��
L��
�����յ�H2��������ɵ�LiH�����Ϊ224L�� ![]() L=1148��1���ʴ��ǣ�1148��1����20molLiH������20molH2 �� ʵ�ʲμӷ�Ӧ��H2Ϊ20mol��80%=16mol��1molH2ת����1molH2O��ת��2mol���ӣ�����16molH2��ת��32mol�ĵ��ӣ����Դ��ǣ�32��
L=1148��1���ʴ��ǣ�1148��1����20molLiH������20molH2 �� ʵ�ʲμӷ�Ӧ��H2Ϊ20mol��80%=16mol��1molH2ת����1molH2O��ת��2mol���ӣ�����16molH2��ת��32mol�ĵ��ӣ����Դ��ǣ�32��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ������Ӻ�ˮ��Դ��ȡijЩ��Ҫ����ԭ�ϵ�����ʾ��ͼ�� 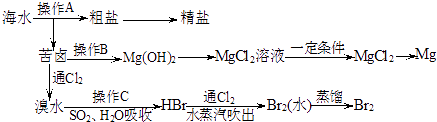
�ش��������⣺
��1������A�����ˣ���ʵ������������ƣ���
��2������B����������Լ��е�һ�֣�����ʵ�����ѡ���ţ���
a������������Һ b������ʯ��ˮ c��ʯ���� d��̼������Һ
��3�����±��ͨ��Cl2 �� ������Ӧ�����ӷ���ʽ�� �� ��SO2ˮ��Һ����Br2 �� �����ʿɴ�95%���йط�Ӧ�����ӷ���ʽΪ ��
��4����ҵ������ˮMgCl2��ȡþ�Ļ�ѧ����ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʽΪC5H12O�ҿ�������Ʒ�Ӧ�ų��������л��������У������������칹��
A. 5�� B. 6�� C. 7�� D. 8��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���¶�t��ʱ��ijNaOHϡ��Һ��c(H��)=10a mol��L1��c(OH)=10b mol��L1����֪a��b=12����ش��������⣺
��1�����¶���ˮ�����ӻ�����KW=________��
��2����NaOH��Һ��NaOH�����ʵ���Ũ��Ϊ_____����NaOH��Һ����ˮ�������c(OH)Ϊ______��
��3������NaOH��Һ���ȣ�pH________(��������С�����䡱)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й�������ԭ��Ӧ��������ȷ���ǣ�������
A. ��һ�������£��������ⷢ����ӦKClO3+I2=2KIO3+Cl2 �ɴ��ж������� I2>Cl2
B. ��֪��Ӧ��2Cu(IO3)2+24KI+12H2SO4=2CuI��+13I2+12K2SO4+12H2O����1mol�������ڷ�Ӧ�еõ��ĵ���Ϊ12 mol
C. (NH4)2SO4�ڸ����·ֽ����� SO2��H2O��N2�� NH3����÷�Ӧ�����������ԭ����=1:3
D. �ڷ�Ӧ2CuFeS2 + O2 = Cu2S + 2FeS + SO2�У�����1molO2�μӷ�Ӧ����Ӧ����4mol����ת��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����Ȫ��Զ�š�ʥˮ��֮����һ����ԡ������Ƥ������ɫ�ߡ��ؽ�����˥�������������Ч��������Ȫ������������ز����ٵ���Ԫ���ǣ� ��
A. Zn��Cu��Mn��Ca B. Fe��Mn��Zn��Mg
C. Zn��Cu��B��Mn D. Mg��Mn��Cu��Mo
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о���Ԫ�ؼ��仯��������ʾ�����Ҫ���塣
��. ��������ȼ�ջ����������������Ҫ�ɷ���SO2��CO2��N2��O2 ��ij�о���ѧϰС����ʵ������������װ���Ʊ�ģ�����������ⶨ������SO2�����������
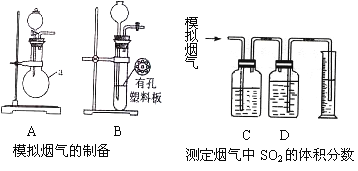
��һ��ģ���������Ʊ�
��1����Aװ����SO2����ѧ��Ӧ����ʽΪ___________________________��
��2����Bװ����CO2��ʹ�ø�װ���ŵ����___________________________��
��3�����Ƶõ������������ֻ�ϣ����ģ���������ں���ʵ�顣
�������ⶨ������SO2���������
��4��������ģ����������ͨ��C��Dװ�ã�����C��D��ʢ�е�ҩƷ�ֱ���__________��__________��������ţ�
��KMnO4��Һ ������NaHSO3��Һ ������Na2CO3��Һ �ܱ���NaHCO3��Һ
��5����ģ������������ΪamL/min����t1���Ӻ����Ͳ��Һ�����ΪVmL����SO2���������____________________��
��.ij��ѧ��ȤС���ͬѧ������ͼ��ʾʵ��װ�ý���ʵ��(ͼ��a��b��c��ʾֹˮ��) ��

��1��A��C��E�������װ�ÿ�������ȡCl2��������ص�����ʵ�顣�����ڱ��м�������ˮ�������Ƶ���ˮ����������ˮ����ʵ�飬ʵ����������������£�
ʵ����� | �� �� | �� �� |
��ˮ�м���̼�����Ʒ�ĩ | ����ɫ���ݲ��� | ������ˮ��Ӧ�IJ���������� |
ʵ��Ľ����Ƿ����__________����ѡ�������������˵������______________________��
������������װ�����һ����ʵ����֤Cl-��S2-�Ļ�ԭ��ǿ��,��ס��ҡ�����ʢ�ŵ��Լ��Ǽ�__________________ ��__________________ ��__________________
��2��B��D��Eװ����������B��ʢװŨ�����ͭƬ(�����п����ϰ���)�����Ƶò�����NO2�й�ʵ�顣����Dװ����֤NO2��ˮ�ķ�Ӧ�����������Ϊ���ȹر�ֹˮ��________���ٴ�ֹˮ��________��ʹ�ձ��е�ˮ�����Թܶ��IJ����ǣ�___________________________________ʹ�Թ��е������ݳ���NO2��ˮ�Ӵ��������ձ��е�ˮ�����Թܶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������A��B��C��D��E�����л�����й���Ϣ��
A | B | C | D | E |
����ʹ��ˮ��ɫ | ����C��H�� | ����C��H��O�� | ����Է������� | ����C��H��O�� |
���ݱ�����Ϣ�ش��������⣺
��1��A����ˮ��Ӧ������������ƽ�����д����һ�������£�A���ɸ߷��ӻ�����Ļ�ѧ����ʽ�� ��
��2��A�����������ӳɷ�Ӧ�����ɷ���F����F�ڷ�����ɺͽṹ�����Ƶ��л�����һ���ࣨ�׳ơ�ͬϵ��������Ǿ�����ͨʽ �� ��n=ʱ�������л��↑ʼ����ͬ���칹�壮
��3��B���е�������������ţ���
����ɫ��ζҺ����ж��۲�����ˮ���ܶȱ�ˮ����κ������²���������Ӧ��ʹ���Ը��������Һ����ˮ����ɫ
д����Ũ���������£�B��Ũ���ᷴӦ�Ļ�ѧ����ʽ�� ��
��4��д����C��������D�Ļ�ѧ����ʽ�� ��
��5��C��E��Ӧ��������Է�������Ϊ100�������÷�Ӧ����Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£���һ�̶�������ܱ������з�����ӦA(s)��3B(g)2C(g)������˵������˵���÷�Ӧ�ﵽ��ѧƽ��״̬����(����)
��C���������ʺ�C�ķֽ��������
�ڵ�λʱ��������a mol A��ͬʱ����3a mol B
�������ܶȲ��ٱ仯
�ܻ���������ѹǿ���ٱ仯
��A��B��C�����ʵ���֮��Ϊ1��3��2
��������ƽ����Է�����������
A. �ڢܢ� B. �٢ۢܢ� C. �٢ڢܢ� D. �٢ڢۢܢ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com