
| A.-44.2kJ?mol-1 | B.+44.2kJ?mlo-1 |
| C.-330kJ?mol-1 | D.+330kJ?mlo-1 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:单选题
| A.pH=3的HNO3跟pH=11的KOH溶液 |
| B.pH=3的盐酸跟pH=11的氨水 |
| C.pH=3硫酸跟pH=11的氢氧化钠溶液 |
| D.pH=3的醋酸跟pH=11的氢氧化钠溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Q1=Q2 | B.Q1>Q2 | C.Q1<Q2 | D.不能确定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.-Y | B.-(10X-Y) | C.-(5X-O.5Y) | D.+(10X-Y) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.4Q1+0.05Q3 | B.0.4Q1+0.05Q2 |
| C.0.4Q1+0.1Q3 | D.0.4Q1+0.1Q2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.X2+2Y2═2XY2 | B.2X2+Y2═2X2Y |
| C.3X2+Y2═2X3Y | D.X2+3Y2═2XY3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.V(A2)=0.01mol/(L?s) | B.V(B2)=1.0mol/(L?min) |
| C.V(AB3)=0.9mol/(L?min) | D.V(A2)=0.8mol/(L?min) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
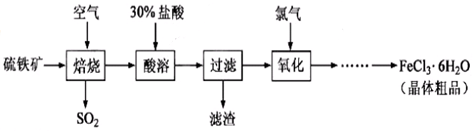
 2SO3(g) ,该反应的平衡常数表达式为K= ;过量的SO2与NaOH溶液反应的化学方程式为
2SO3(g) ,该反应的平衡常数表达式为K= ;过量的SO2与NaOH溶液反应的化学方程式为 查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com