
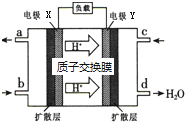
 绿色电源“二甲醚-氧气燃料电池”的工作原理如图,
绿色电源“二甲醚-氧气燃料电池”的工作原理如图,

科目:高中化学 来源: 题型:
| A、Na+、Al3+、HCO3-、NO3- |
| B、AlO2-、Mg2+、H+、K+ |
| C、NH4+、Na+、CH3COO-、NO3- |
| D、Na+、NO3-、ClO-、I- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| A、电池放电时,电池负极周围的溶液pH不断增大 |
| B、电池放电时,镍元素被氧化 |
| C、电池放电时,镍元素被还原 |
| D、电池放电时,H2是负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:
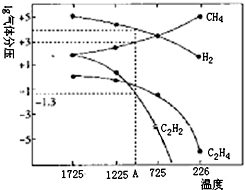 乙炔(C2H2)在气焊、气割及有机合成中用途非常广泛,可由电石(CaC2)直接水化法或甲烷在1500℃左右气相裂解法生产.
乙炔(C2H2)在气焊、气割及有机合成中用途非常广泛,可由电石(CaC2)直接水化法或甲烷在1500℃左右气相裂解法生产.查看答案和解析>>
科目:高中化学 来源: 题型:
| X | Y | ||
| Z | W |
| A、原子半径Z>W>Y |
| B、最高价氧化物对应水化物的酸性Z>W |
| C、氢化物的稳定性X>Z |
| D、X的氢化物与Y的氢化物能发生化合反应生成离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
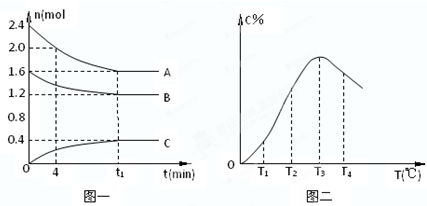
| A、0~4分钟时,A的速率为0.01mol/(L?min) | ||
| B、由T1向T2变化时,V正>V | ||
C、该反应的平衡常数表达式K=
| ||
| D、此反应的正反应为吸热反应. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com