

| ||
| ||
| ||
| ||


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、称取2.0gNaOH,加入480ml水 |
| B、称取2.0gNaOH,配制480mL溶液 |
| C、称取2.0gNaOH,加入500mL水 |
| D、称取2.0gNaOH,配制500mL溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 13 |
| 2 |
| 13 |
| 2 |
| 9 |
| 2 |
| 9 |
| 2 |
| A、-2878kJ/mol |
| B、-2658kJ/mol |
| C、-1746kJ/mol |
| D、-1526kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、油脂发生皂化反应能生成甘油 |
| B、蔗糖及其水解产物均能与新制氢氧化铜反应生成红色沉淀 |
| C、实验室可以使用CuSO4溶液除去乙炔中的H2S等杂质 |
| D、甲烷、苯、乙醇、乙酸和乙酸乙酯都可以发生取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 陈述I | 陈述Ⅱ | |
| A | 常温下铁、铜均不溶于浓硫酸 | 常温下铁、铜与浓硫酸均不反应 |
| B | HCl与Na2CO3溶液反应生成CO2 | 用饱和Na2CO3溶液除去CO2中的少量HCl |
| C | Cl2使润湿的有色布条褪色,而干燥的布条不褪色 | 次氯酸的氧化性比氯气的强 |
| D | 稀、浓HNO3分别与铜反应,还原产物为NO和NO2 | 稀HNO3氧化性比浓HNO3强 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
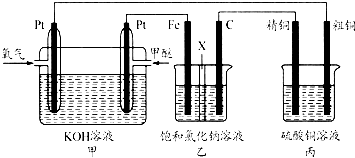
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | Cl2 | Br2 | I2 | H2 | HF | HCl | HBr | HI |
| 能量(kJ) | 243 | 193 | 151 | 436 | 568 | 431 | 366 | 298 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、使甲基橙呈红色的溶液中K+、Na+、NO3-、S2O32- |
| B、NH4+、Fe3+、CO32-、CH3COO- |
| C、使酚酞变红色的溶液中:Na+、Cl-、K+、AlO2- |
| D、无色透明溶液中:SO32-、Cl-、K+、Cr2O72- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质类别 | 酸 | 碱 | 盐 | 氧化物 |
| 化学式 | ①HCl ② | ③ ④Ba(OH)2 | ⑤Na2CO3 ⑥ | ⑦CO2 ⑧Na2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com