
Į÷¶Æµē³ŲŹĒŅ»ÖÖŠĀŠĶµē³Ų”£ĘäÖ÷ŅŖĢŲµćŹĒæÉŅŌĶعżµē½āÖŹČÜŅŗµÄŃ»·Į÷¶Æ£¬ŌŚµē³ŲĶā²æµ÷½Śµē½āÖŹČÜŅŗ£¬ŅŌ±£³Öµē³ŲÄŚ²æµē¼«ÖÜĪ§ČÜŅŗÅØ¶ČµÄĪČ¶Ø”£±±¾©»Æ¹¤“óѧŠĀæŖ·¢µÄŅ»ÖÖĮ÷¶Æµē³ŲČēĶ¼ĖłŹ¾£¬µē³Ų×Ü·“Ó¦ĪŖCu£«PbO2£«2H2SO4=CuSO4£«PbSO4£«2H2O”£ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
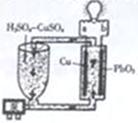
A.aĪŖøŗ¼«£¬bĪŖÕż¼« B.øƵē³Ų¹¤×÷Ź±PbO2µē¼«ø½½üČÜŅŗµÄpHŌö“ó
C.a¼«µÄµē¼«·“Ó¦ĪŖCu£2e£=Cu2£« D.µ÷½Śµē½āÖŹČÜŅŗµÄ·½·ØŹĒ²¹³äCuSO4
”¾ÖŖŹ¶µć”æŌµē³ŲŌĄķµÄÓ¦ÓĆ F3
”¾“š°ø½āĪö”æD ½āĪö£ŗA. øł¾Żµē³Ų×Ü·“Ó¦£ŗCu£«PbO2£«2H2SO4=CuSO4£«PbSO4£«2H2OæɵĆĶ×öĪŖøŗ¼«£¬PbO2ĪŖÕż¼«£¬ÕżČ·£»B.øƵē³Ų¹¤×÷Ź±PbO2µē¼«·¢ÉśµÄ·“Ó¦ĪŖ£ŗ PbO2£«4H++SO42—=PbSO4£«2H2O£¬ĻūŗÄĮĖČÜŅŗÖŠµÄH+£¬¹ŹČÜŅŗµÄpHŌö“ó£¬ÕżČ·£»C.Ķµē¼«µÄµē¼«·“Ó¦ĪŖCu£2e£=Cu2£«£¬ÕżČ·£»D.Ķعż×Ü·“Ó¦æÉŅŌ擵½H2SO4²Ī¼ÓĮĖ·“Ó¦£¬¹ŹÓ¦²¹³äH2SO4£¬“ķĪó”£
”¾Ė¼Ā·µć²¦”æ±¾Ģāæ¼²éĮĖŌµē³ŲŌĄķµÄÓ¦ÓĆ£¬µē¼«µÄÅŠ¶ĻŗĶµē¼«·“Ó¦µÄŹéŠ“ŹĒ±¾Ģāæ¼²éµÄÖŲµć£¬ÄѶČÖŠµČ”£


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Č”“ś·“Ó¦ŹĒÓŠ»ś»Æѧ֊Ņ»ĄąÖŲŅŖµÄ·“Ó¦£¬ĻĀĮŠ·“Ó¦ŹōÓŚČ”“ś·“Ó¦µÄŹĒ(””””)
A£®±ūĶéÓėĀČĘųŌŚ¹āÕÕĢõ¼žĻĀÉś³ÉĀȱūĶé
B£®ŅŅĻ©ÓėäåµÄĖÄĀČ»ÆĢ¼ČÜŅŗ·“Ӧɜ³É1,2¶žäåŅŅĶé
C£®ŅŅĻ©ÓėĖ®·“Ӧɜ³ÉŅŅ“¼
D£®ŅŅĻ©×ŌÉķ¾ŪŗĻÉś³É¾ŪŅŅĻ©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠ·ÖĪö·½·Ø²»ŹĒĻÖ“ś»Æѧ²ā¶ØÓŠ»śĪļ½į¹¹µÄ·½·ØµÄŹĒ(””””)
A£®Č¼ÉÕ·Ø B£®ŗģĶā¹āĘ×·Ø
C£®×ĻĶā¹āĘ×·Ø D£®ŗĖ“Ź²Õń·Ø
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ijӊ»śĪļ3.24 g×°ČėŌŖĖŲ·ÖĪö×°ÖĆ£¬ĶØČė×ćĮæµÄŃõĘųŹ¹Ö®ĶźČ«Č¼ÉÕ£¬½«Éś³ÉµÄĘųĢåŅĄ“ĪĶعżĪŽĖ®CaCl2(A)¹ÜŗĶ¼īŹÆ»Ņ(B)¹Ü£¬²āµĆA¹ÜŌöÖŲ2.16 g£¬B¹ÜŌöÖŲ9.24 g£¬ŅŃÖŖøĆÓŠ»śĪļµÄĻą¶Ō·Ö×ÓÖŹĮæŠ”ÓŚ200”£ĒóøĆÓŠ»śĪļµÄ×ī¼ņŹ½ŗĶ»ÆѧŹ½”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
£Ø1£©2.00g C2H2ĶźČ«Č¼ÉÕÉś³ÉŅŗĢ¬Ė®ŗĶCO2£¬·Å³ö99.6kJČČĮ棬ĒėŠ“³ö±ķŹ¾C2H2Č¼ÉÕČȵÄČČ»Æѧ·½³ĢŹ½£ŗ
£Ø2£©C2H2æÉÓĆÓŚÖĘ×÷Č¼ĮĻµē³Ų£¬ĒėŠ“ŅŌKOHČÜŅŗĪŖµē½āÖŹČÜŅŗµÄŅŅČ²Č¼ĮĻµē³ŲµÄøŗ¼«·“Ó¦Ź½£ŗ
£Ø3£©ÓĆŅŅČ²Č¼ĮĻµē³Ųµē½āAgNO3ČÜŅŗ£¬ÓĆŹÆÄ«×öµē½ā³ŲĮ½¼«£¬ĒėŠ“³öÓėµēŌ“øŗ¼«ĻąĮ¬µÄŹÆÄ«µē¼«µÄµē¼«·“Ó¦Ź½£ŗ
£Ø4£©øßĢśµē³ŲŹĒŅ»ÖÖŠĀŠĶæɳäµēµē³Ų£¬ÓėĘÕĶØøßÄܵē³ŲĻą±Č£¬øƵē³ŲÄܳ¤Ź±¼ä±£³ÖĪČ¶ØµÄ·ÅµēµēŃ¹”£øßĢśµē³ŲµÄ×Ü·“Ó¦ĪŖ£ŗ
3Zn + 2K2FeO4 + 8H2O  3Zn(OH)2 + 2Fe(OH)3 + 4KOH
3Zn(OH)2 + 2Fe(OH)3 + 4KOH
ĒėŠ“³öøƵē³ŲŌŚ³äµēŹ±Ņõ¼«µÄµē¼«·“Ó¦Ź½£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
2010Äź4ŌĀ֊ѮȫĒņŗĖ°²Č«·å»įŌŚ»ŖŹ¢¶Ł¾ŁŠŠ£¬·¢Õ¹ŗĖµē”¢ÖĘ²ĆŗĖĪäĘ÷·¢Õ¹ŹĒ»įŅéÖ÷Ģā£¬ø÷Ź½ø÷Ńłµē³ŲµÄ·¢Õ¹ŹĒ»Æѧ¶ŌČĖĄąµÄŅ»ĻīÖŲ“ó¹±Ļ×£¬ĻĀĮŠÓŠ¹Ųµē³ŲµÄŠšŹöÕżČ·µÄŹĒ
A£®ŹÖ»śÉĻÓƵÄļ®Ąė×Óµē³ŲŹōÓŚŅ»“Īµē³Ų
B£®ŠæĆĢøɵē³ŲÖŠ£¬Šæµē¼«ŹĒøŗ¼«
C£®ĒāŃõČ¼ĮĻµē³Ų¹¤×÷Ź±ĒāĘųŌŚøŗ¼«±»»¹Ō
D£®Ģ«ŃōÄܵē³ŲµÄÖ÷ŅŖ²ÄĮĻĪŖ¶žŃõ»Æ¹č
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ijĮņĖį³§ŅŌŗ¬ÓŠSO2µÄĪ²Ęų”¢°±Ė®µČĪŖŌĮĻ£¬ŗĻ³ÉÓŠÖŲŅŖÓ¦ÓĆ¼ŪÖµµÄĮņ»ÆøĘ”¢ĮņĖį¼Ų”¢ŃĒĮņĖįļ§µČĪļÖŹ”£ŗĻ³ÉĀ·ĻßČēĻĀ:
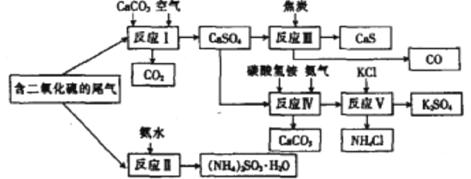
(1)Š“³ö·“Ó¦¢óµÄ»Æѧ·½³ĢŹ½:
(2)ĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ (Ģī×ÖÄø)”£
A·“Ó¦¢ńÖŠŠč¹ÄČė×ćĮææÕĘų£¬ŅŌ±£Ö¤¶žŃõ»ÆĮņ³ä·ÖŃõ»ÆÉś³ÉĮņĖįøĘ
B.·“Ó¦¢ņŗĶ·“Ó¦¢óµÄ»ł±¾·“Ó¦ĄąŠĶĻąĶ¬
C.·“Ó¦¢ōŠčæŲÖĘŌŚ60-70”ę£¬ÄæµÄÖ®Ņ»ŹĒ¼õÉŁĢ¼ĖįĒāļ§µÄ·Ö½ā
D.·“Ó¦¢õÖŠµÄø±²śĪļĀČ»Æļ§æÉÓĆ×÷µŖ·Ź
(3) (NH4 )2SO3æÉÓĆÓŚµē³§µČŃĢµĄĘųÖŠĶѵŖ£¬½«µŖŃõ»ÆĪļ×Ŗ»ÆĪŖµŖĘų£¬Ķ¬Ź±Éś³ÉŅ»ÖÖµŖ·Ź£¬ŠĪ³É¹²ÉśĻµĶ³”£Š“³ö¶žŃõ»ÆµŖÓėŃĒĮņĖįļ§·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ .
(4)ŗܶąĮņĖį³§ĪŖ»ŲŹÕĄūÓĆSO2£¬Ö±½ÓÓĆ°±Ė®ĪüŹÕ·Ø“¦ĄķĪ²Ęų.
¢ŁÓĆ15. 0mL 2.0mol·L-1°±Ė®ĪüŹÕ±ź×¼×“æöĻĀ448 mL SO2£¬ĪüŹÕŅŗÖŠµÄČÜÖŹĪŖ
¢ŚÄ³Ķ¬Ń§ÓĆĖįŠŌKMnO4ČÜŅŗµĪ¶ØÉĻŹöĪüŹÕŅŗ£¬µ±“ļµ½µĪ¶ØÖÕµćŹ±£¬ĻūŗÄKMnO4ČÜŅŗ25. 00 mL£¬ŌņĖįŠŌKMnO4ČÜŅŗÖŠ£¬c(KMnO4)=
(5)°±ĘųÓĆĶ¾¹ć·ŗ£¬æÉŅŌÖ±½ÓÓĆÓŚČ¼ĮĻµē³Ų£¬ÓŅĶ¼ŹĒÓĆ°±Ė®×÷Č¼ĮĻµÄČ¼ĮĻµē³ŲµÄ¹¤×÷ŌĄķ”£
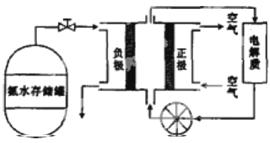
°±ĘųČ¼ĮĻµē³ŲµÄµē½āÖŹČÜŅŗ×īŗĆŃ”Ōń (Ģī”°ĖįŠŌ”±”°¼īŠŌ”±»ņ”°ÖŠŠŌ”±)ČÜŅŗ£¬µŖĘųČ¼ĮĻµē³ŲµÄ·“Ó¦ŹĒ°±ĘųÓėŃõĘųÉś³ÉŅ»ÖÖ³£¼ūµÄĪŽ¶¾ĘųĢåŗĶĖ®£¬øƵē³Ų×Ü·“Ó¦µÄ»Æѧ·½³ĢŹ½
ŹĒ_______________________________£¬øŗ¼«µÄµē¼«·“Ó¦Ź½ŹĒ_______________________________
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
A”¢B”¢C”¢X¾łĪŖ֊ѧ»Æѧ³£¼ūµÄĪļÖŹ£¬ĖüĆĒÖ®¼äÓŠČēĻĀ×Ŗ»Æ¹ŲĻµ(ĘäĖü²śĪļŅŃĀŌČ„)£ŗ

ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
A.ČōAŹĒNH3ŌņCæÉÄÜŹĒŃõ»ÆĪļ
B.ČōAŹĒ·Ē½šŹōµ„ÖŹ£¬ŌņCÓėĖ®·“Ó¦µÄÉś³ÉĪļĪŖĒæĖį
CČōXŹĒ½šŹōµ„ÖŹ£¬ŌņB”¢C ÖŠXµÄ»ÆŗĻ¼ŪæÉÄÜŹĒB>C
D.ČōXŹĒĒæ¼ī£¬ŌņBæÉÄÜŹĒĮ½ŠŌĪļÖŹ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŌŚČŻ»żĪŖ1 LµÄĆܱÕČŻĘ÷ÖŠ£¬¼ÓČė5 mol AĪļÖŹ£¬ŌŚŅ»¶ØĢõ¼žĻĀĶ¬Ź±·¢ÉśĻĀĮŠĮ½øö·“Ó¦£ŗ(1)2A(g)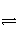
 2B(g)£«C(g)£»(2)A(g)
2B(g)£«C(g)£»(2)A(g)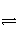
 C(g)£«D(g)”£µ±“ļµ½Ę½ŗāŹ±£¬²āµĆ[A]£½2.5 mol”¤L£1£¬[C]£½2.0 mol”¤L£1”£ŌņĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ(””””)
C(g)£«D(g)”£µ±“ļµ½Ę½ŗāŹ±£¬²āµĆ[A]£½2.5 mol”¤L£1£¬[C]£½2.0 mol”¤L£1”£ŌņĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ(””””)
A£®“ļµ½Ę½ŗāŹ±AµÄ×Ü×Ŗ»ÆĀŹĪŖ40%
B£®“ļµ½Ę½ŗāŹ±[B]ĪŖ1.0 mol”¤L£1
C£®“ļµ½Ę½ŗāŹ±[B]£½2[D]
D£®“ļµ½Ę½ŗāŹ±[D]£½2[B]
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com