
����Ŀ��������30mLͬһŨ�ȵ�NaOH��Һ��ͨ��CO2���壬��CO2ͨ�����IJ�ͬ����Һ�����Ҳ��ͬ���õ���ҺM��N������M��N��Һ����μ���Ũ��Ϊ0.25mol��L��1���ᣬ�������������v(CO2)�������������v(HCl)�Ĺ�ϵ�ֱ�Ϊ��ͼ��ʾ�������A��B��
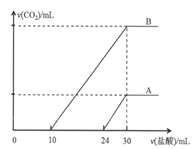
��ش��������⣺
��1��M��Һ������Ϊ(д��ѧʽ)___________�������ʵ���֮����__________��
��2��N��Һ����Ϊ(д��ѧʽ)____________����״����CO2��������Ϊ________��ԭNaOH��Һ�����ʵ���Ũ��Ϊ_________ ��
���𰸡� NaOH��Na2CO3 3:1 Na2CO3��NaHCO3 112mL 0.25mol/L
�����������ݶ�����̼ͨ������������Һ�п��ܵIJ�����̼���ơ�̼�����ơ�ˮ��M��N����Һ�м���������Һ���Ⱥ����ķ�ӦΪ��HCl+NaOH=NaCl+H2O����Na2CO3+HCl=NaHCO3+NaCl����NaHCO3+HCl=NaCl+CO2+H2O��
��1���������A��M��Һ�з����ķ�Ӧ�����٢ڢ���M�е�����ΪNaOH��Na2CO3�����A��24~30�η����ķ�ӦΪ�ۣ��ٸ��ݷ�Ӧ�ڿ�֪����Һ��̼�������ĵ�������������Ϊ6 mL��˵��̼���Ƶ����ʵ���Ϊ0.006 L![]() 0.25mol��L��1=0.0015mol������������������������Ϊ24-6=18mL�����ݷ�Ӧ�ٿ�֪�������Ƶ����ʵ���Ϊ0.018 L
0.25mol��L��1=0.0015mol������������������������Ϊ24-6=18mL�����ݷ�Ӧ�ٿ�֪�������Ƶ����ʵ���Ϊ0.018 L![]() 0.25mol��L��1=0.0045mol�����������ƺ�̼���Ƶ����ʵ���֮��Ϊ3:1��
0.25mol��L��1=0.0045mol�����������ƺ�̼���Ƶ����ʵ���֮��Ϊ3:1��
��2����ͼ��֪��������������Ϊ30mLʱ�����ٲ������壬ǡ���γ��Ȼ�����Һ���������Ƶ�Ũ�ȵ��������Ũ��Ϊ0.25mol��L��1���ٸ������B��֪��10~30mLΪ̼�����������ᷴӦ������Һ��̼����ת��Ϊ̼�����������ĵ���������ֻ��10mL������������̼�����Ʋ��ܹ��棬˵��N�е�����ΪNa2CO3��NaHCO3��10~30mL�����ķ�Ӧ�ۣ�����CO2��������ʵ���Ϊ0.02 L![]() 0.25mol��L��1=0.005mol���������������Ϊ112 mL��
0.25mol��L��1=0.005mol���������������Ϊ112 mL��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵���в���ȷ���ǣ� ��
A.�����ͬ��c��Na+����ȵĴ�����Һ��С�մ���Һ���ֱ�������ͬ�����ᷴӦ�����������������
B.��ͭ�ۼ����Ȼ�����Һ����ַ�Ӧ����������ʣ�࣬��ù��岻���ܺ���
C.��AlCl3��Һ��ȡAl��OH��3 �� ������ѡ�ð�ˮ��ѡ��NaOH��Һ��
D.��ͬ�������ơ�þ�����ֱ���������ϡ���ᷴӦ���������������֮��Ϊ27��24��23
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵���в���ȷ���ǣ� ��
A.�����ͬ��c��Na+����ȵĴ�����Һ��С�մ���Һ���ֱ�������ͬ�����ᷴӦ�����������������
B.��ͭ�ۼ����Ȼ�����Һ����ַ�Ӧ����������ʣ�࣬��ù��岻���ܺ���
C.��AlCl3��Һ��ȡAl��OH��3 �� ������ѡ�ð�ˮ��ѡ��NaOH��Һ��
D.��ͬ�������ơ�þ�����ֱ���������ϡ���ᷴӦ���������������֮��Ϊ27��24��23
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����н�������A��B��C������ס��ҡ���������D��E��F��G��H������֮���ܷ������·�Ӧ��ͼ����Щ��Ӧ�IJ���ͷ�Ӧ������û��ȫ���������

�����������Ϣ�ش��������⣺
��1��д������Ԫ��A��ԭ�ӽṹʾ��ͼ��_______________��
��2��д�����з�Ӧ�����ӷ���ʽ����Ӧ��_____________
��Ӧ��________________
��3����������G�������ӵIJ�������_________________________________________��
��4����������F����Һʱ��Ҫ����____________��Ŀ����______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪A��B��C��D����ǿ�������Һ���ֱ����������������еĸ�һ�֣��һ����ظ���Ba2+��H+��Na+��NH4+��CO32����NO3����SO42����OH�� �� ��֪����A��B��Ӧ���ɵ������ܱ�D���գ���A��D��Ӧ���ɵ������ܱ�B���գ�����A��D�е���C�����а�ɫ�������������о���E��Ħ������Ϊ474g/mol������������ˮ�ľ�ˮ�������жϣ�
��1������E������Ϊ �� �����ӷ���ʽ�ͱ�Ҫ������˵��E��������ˮ����ԭ�� ��
��2��д��A��B��C�Ļ�ѧʽ��A �� B �� C ��
��3��д��A��D��Ӧ�����ӷ���ʽ ��
��4����200mL0.5mol/L��B��Һ���뵽150mL0.2mol/L��E��Һ�У��������ɵİ�ɫ��������Ϊg��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йػ��������������У��������
A.�������������������ˮ�����ŷſ�ʹˮ�帻Ӫ����
B.��ҵ�����ŷŶ���������ȫ�������ů����Ҫԭ��
C.ijЩװ�����к��еļ�ȩ�����Ȼ�����Ӱ�����彡��
D.�Ͼɵ���к��еĹ���Ǧ���ӵ��ؽ����ζ�������ˮԴ�������Ⱦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����2H2�� g ��+O2�� g ��=2H2O �� l ������H=��572kJ/mol
��2H2�� g ��+O2�� g ��=2H2O �� g ������H=��484kJ/mol
��CH4 �� g ��+2O2�� g ��=2H2O �� l ��+CO2�� g ������H=��890kJ/mol
��1����֪H��H�ļ���436kJ/mol O=O�ļ���496kJ/mol H��O�ļ���463kJ/mol�������������ݼ���٢���һ����Ӧ����ͨ������ֱ�Ӽ���ó� �� ������д����Ӧ H2O �� l ��=H2O �� g �����ʱ��H= ��
��2���������ɼ���CO2��g��+4H2�� g ��=CH4�� g ��+2H2O�� g �����ʱ��H= ��
��3���ڢ٢ڢ���������ʽ����һ����ȼ���ȵ��Ȼ�ѧ����ʽ �� ���Ӧ����ʽ����ţ�
��״���£�ȡ����������Ļ������11.2L��ȫȼ�պ�ָ������£���ų�������Ϊ26��3.8kJ�������������м������������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���H��һ�����ϣ��ɴӸ�������������ȡ������һ�ֺϳ�·������ 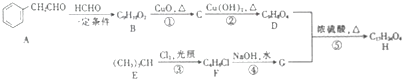
��֪��
��D����̼��������Һ��Ӧ
��G�˴Ź���������ʾ������к���2�ֲ�ͬ��ѧ��������ԭ�ӣ�
��CH3CHO+CH3CHO ![]()
![]()
�ش��������⣺
��1��A��B�ķ�Ӧ����Ϊ
��2��E������ΪF�Ľṹ��ʽΪ
��3����Ӧ�ٵĻ�ѧ����ʽΪ
��4����Ӧ�ݵĻ�ѧ����ʽΪ
��5��D�ж���ͬ���칹�壬д����������������D������ͬ���칹��Ľṹ��ʽ���������������칹�� I�������Ϻ�������ȡ����
������NaHCO3��Һ��Ӧ
���ܷ���������Ӧ��ˮ�ⷴӦ
IV���˴Ź���������4���
��6�����������ϳ�·�ߣ����һ����AΪԭ���Ʊ�  �ĺϳ�·�ߣ�
�ĺϳ�·�ߣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ᶼ����Ҫ�Ļ���ԭ�ϣ�Ҳ�ǻ�ѧʵ������ر�����Ҫ�Լ���
��1�������£��������������Ƶ�����ʢ��Ũ���ᣬ˵��Ũ�������________�ԡ�
A������ B��ǿ������ C����ˮ�� D����ˮ��
��2����ҵ����ϴ���ķ�ͭм��ԭ�����Ʊ�����ͭ�������Ʊ��������ϡ���ɫ��ѧ��˼�����_______������ţ���
��Cu+H2SO4(Ũ)��CuSO4 ��Cu![]() CuO
CuO![]() CuSO4
CuSO4
д�����з�Ӧ�Ļ�ѧ����ʽ��_____________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com