

 的含氧官能团的名称为醚键和羧基、羟基
的含氧官能团的名称为醚键和羧基、羟基 .
. 分析 根据题中各物质转化关系,CH2=CH2与溴发生加成反应生成A为CH2BrCH2Br,在碱性条件下发生水解得CH2OHCH2OH,发生氧化反应得B为OHCCHO,B再氧化得OHCCOOH,反应③的反应物的原子利用率为100%,所以OHCCOOH与 发生加成反应得
发生加成反应得 ,据此答题.
,据此答题.
解答 解:根据题中各物质转化关系,CH2=CH2与溴发生加成反应生成A为CH2Br=CH2Br,在碱性条件下发生水解得CH2OHCH2OH,发生氧化反应得B为OHCCHO,B再氧化得OHCCOOH,反应③的反应物的原子利用率为100%,所以OHCCOOH与 发生加成反应得
发生加成反应得 ,
,
(1)根据 的结构简式可知,其中含氧官能团的名称为醚键和羧基、羟基,故答案为:羧基、羟基;
的结构简式可知,其中含氧官能团的名称为醚键和羧基、羟基,故答案为:羧基、羟基;
(2)反应①为CH2BrCH2Br在碱性条件下发生水解得CH2OHCH2OH,所以反应的条件为NaOH溶液、加热,故选b;
(3)反应②的化学方程式为HOCH2-CH2OH+O2$→_{△}^{Cu}$OHC-CHO+2H2O,故答案为:HOCH2-CH2OH+O2$→_{△}^{Cu}$OHC-CHO+2H2O;
(4)根据上面的分析可知,反应③的类型为加成反应,比较 和OHCCOOH的结构,反应③的另一种反应物的结构简式为
和OHCCOOH的结构,反应③的另一种反应物的结构简式为 ,
,
故答案为:加成反应; .
.
点评 本题考查有机物的合成,为考高常见题型,侧重于学生的分析能力的考查,注意把握官能团的性质,本题可从正向推断,注意把握题给信息.


科目:高中化学 来源: 题型:选择题

| A. | 丙与戊的原子序数相差28 | |
| B. | 气态氢化物的稳定性:庚<己<戊 | |
| C. | 常温下,庚和乙形成的化合物易溶于水 | |
| D. | 丁的最高价氧化物不与任何酸反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,关于该有机物下列叙述正确的是( )
,关于该有机物下列叙述正确的是( )| A. | 不能使酸性KMnO4溶液褪色 | |
| B. | 不能使溴水褪色 | |
| C. | 在加热和催化剂作用下,最多能和3mol H2反应 | |
| D. | 一定条件下,不能和NaOH醇溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 直馏汽油能使溴水因化学反应而褪色 | |
| B. | 常温下,含碳量最高的气态烃是乙炔 | |
| C. | 石油的分馏可以得到汽油、煤油、柴油 | |
| D. | 芳香烃主要来自于煤的干馏后的煤焦油 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
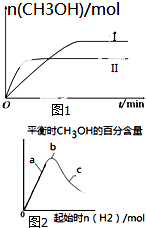 研究CO2的利用对促进低碳社会的构建具有重要的意义.
研究CO2的利用对促进低碳社会的构建具有重要的意义.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2SO4和NaCl的物质的量之比为1:8 | |
| B. | 溶液中一定有0.1molNa2SO4和0.8molNaCl | |
| C. | SO42-所带电荷数是Na+的0.8倍 | |
| D. | SO42- 与Cl-的物质的量之和等于Na+的物质的量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在碳酸氢镁溶液中加入足量Ca(OH)2溶液:Mg2++HCO3-+Ca2++2OH-═MgCO3↓+CaCO3↓+2H2O | |
| B. | 向饱和碳酸钠溶液通入过量的二氧化碳气体:CO32-+CO2+H2O═2HCO3- | |
| C. | 将氯化亚铁溶液和稀硝酸混合:3Fe2++4H++NO3-═3Fe3++2H2O+NO↑ | |
| D. | 向明矾溶液中逐滴加入Ba(OH)2溶液至Al3+刚好沉淀完全:Al3++SO42-+Ba2++3OH-═BaSO4↓+Al(OH)3↓ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com