
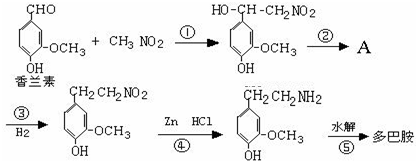
 .
. ,
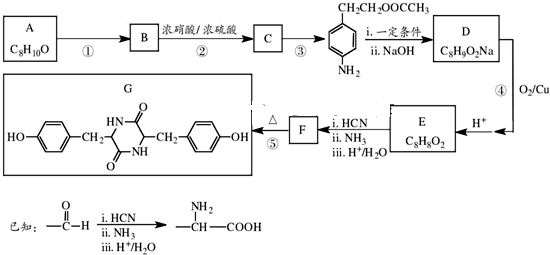
, 反应生成A,A和氢气加成生成
反应生成A,A和氢气加成生成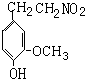 ,将
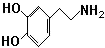
,将 和
和 比较知,
比较知, 先发生消去反应生成A,A再和氢气发生加成反应生成
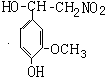
先发生消去反应生成A,A再和氢气发生加成反应生成 ,所以A的结构简式为
,所以A的结构简式为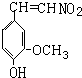 ,
, 和Zn、HCl发生还原反应生成
和Zn、HCl发生还原反应生成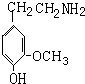 ,
,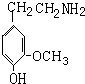 发生水解也是取代反应生成多巴胺,据此答题.
发生水解也是取代反应生成多巴胺,据此答题. ,
, 反应生成A,A和氢气加成生成
反应生成A,A和氢气加成生成 ,将
,将 和
和 比较知,
比较知, 先发生消去反应生成A,A再和氢气发生加成反应生成
先发生消去反应生成A,A再和氢气发生加成反应生成 ,所以A的结构简式为
,所以A的结构简式为 ,
, 和Zn、HCl发生还原反应生成
和Zn、HCl发生还原反应生成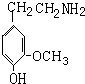 ,
,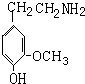 发生水解也是取代反应生成多巴胺,
发生水解也是取代反应生成多巴胺,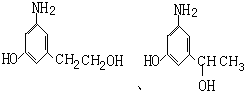 ,
,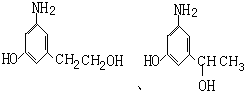 ;
; ,A与足量浓溴水反应的化学方程式为
,A与足量浓溴水反应的化学方程式为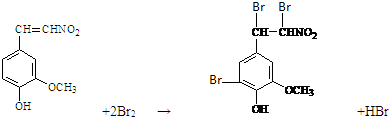 ,
, .
.


 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案科目:高中化学 来源: 题型:
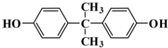 )与光气(
)与光气(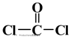 )聚合得到,请写出该聚碳酸酯的结构简式
)聚合得到,请写出该聚碳酸酯的结构简式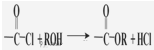 )
)查看答案和解析>>
科目:高中化学 来源: 题型:
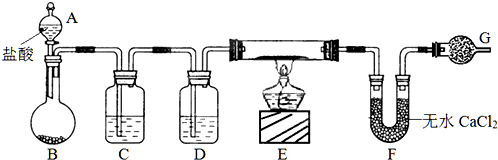
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验次数 | 镁带质量(g) | 测得气体的体积(L) |
| 1 | 18.000 | 16.90 |
| 2 | 18.000 | 17.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:
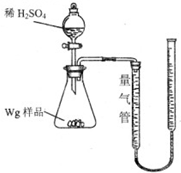 用如图所示装置测定Fe和Fe2O3的混合物中单质铁的质量分数(夹持部分已略去).称取Wg样品置于锥形瓶中,通过分液漏斗加入足量稀硫酸使样品完全溶解.实验前量气管起始读数为amL,实验后量气管的最终读数为bmL.
用如图所示装置测定Fe和Fe2O3的混合物中单质铁的质量分数(夹持部分已略去).称取Wg样品置于锥形瓶中,通过分液漏斗加入足量稀硫酸使样品完全溶解.实验前量气管起始读数为amL,实验后量气管的最终读数为bmL.| 序号 | 溶液中可能存在 的金属离子 | 选择最少种数的试剂,验证该 假设(填字母) |
| ① | ||
| ② | ||
| ③ |
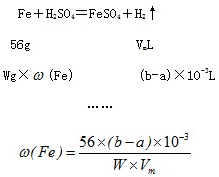
查看答案和解析>>
科目:高中化学 来源: 题型:
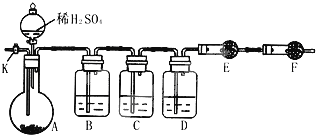
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、8mL | B、8.5mL |
| C、l0mL | D、12mL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com