
| 序号 | 待测物质 | 加入试剂 | 操作方法 |
| ① | 乙醛(乙酸) | NaOH溶液 | |
| ② | CH3CH2OH(水) | ||
| ③ | 苯(苯酚) | ||
| ④ | 乙酸乙酯(乙酸) |
分析 ①乙酸与NaOH溶液反应后,增大与乙醛的沸点差异;
②加CaO与水反应后,增大与乙醇的沸点差异;
③苯酚与NaOH溶液反应后,与苯分层;
④乙酸与饱和碳酸钠溶液反应后,与乙酸乙酯分层.
解答 解:①乙酸与NaOH溶液反应后,增大与乙醛的沸点差异,则选择分离方法为蒸馏;
②加CaO与水反应后,增大与乙醇的沸点差异,则加入试剂为CaO,分离方法为蒸馏;
③苯酚与NaOH溶液反应后,与苯分层,则加入试剂为NaOH溶液,分离方法为分液;
④乙酸与饱和碳酸钠溶液反应后,与乙酸乙酯分层,则加入试剂为饱和碳酸钠溶液,分离方法为分液,
故答案为:
| 序号 | 待测物质 | 加入试剂 | 操作方法 |
| ① | 乙醛(乙酸) | NaOH溶液 | 蒸馏 |
| ② | CH3CH2OH(水) | CaO | 蒸馏 |
| ③ | 苯(苯酚) | NaOH溶液 | 分液 |
| ④ | 乙酸乙酯(乙酸) | 饱和碳酸钠溶液 | 分液 |
点评 本题考查物质分离提纯的方法和选择,为高频考点,把握物质的性质、性质差异及发生的反应为解答的关键,侧重分析与实验能力的考查,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它能使酚酞试液变红色 | |
| B. | 氨水极易挥发出氨 | |
| C. | 氨与水结合生成的一水合氨(NH3•H2O)只有小部分电离成NH4+和OH- | |
| D. | 溶于水的氨大部分以NH3分子形式存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 聚乙烯塑料的老化是由于发生了加成反应 | |
| B. | 煤经过气化和液化等物理变化可以转化为清洁燃料 | |
| C. | 合成纤维、人造纤维及碳纤维都属于有机高分子材料 | |
| D. | 乙烯和苯都能使溴水褪色,褪色的原因不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 该化合物仅含碳、氢两种元素 | B. | 该化合物中碳、氢原子个数比为1:4 | ||
| C. | 无法确定该化合物是否含有氧元素 | D. | 此有机物的最简式为CH4O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
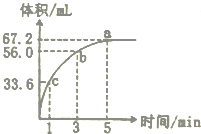 某“学习小组”研究影响化学反应速率的因素.向10 mL某浓度的H2O2溶解中加入一定量MnO2粉末,在标准状况下放出气体的体积和时间的关系如图所示,
某“学习小组”研究影响化学反应速率的因素.向10 mL某浓度的H2O2溶解中加入一定量MnO2粉末,在标准状况下放出气体的体积和时间的关系如图所示,查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com