
 3C(g)+D(g)达平衡时,C的浓度为Wmol/L。若维持容器体积和温度不变,按下列四种配比作为起始物质,达平衡后,C的浓度仍为Wmol/L的是
3C(g)+D(g)达平衡时,C的浓度为Wmol/L。若维持容器体积和温度不变,按下列四种配比作为起始物质,达平衡后,C的浓度仍为Wmol/L的是 科目:高中化学 来源: 题型:阅读理解
| T(K) | 938 | 1100 |
| K | 0.68 | 0.40 |
| c(CO2) |
| c(CO) |
| c(CO2) |
| c(CO) |
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
| 一定条件 |
| 0.082 |
| 0.06×0.183 |
| 0.082 |
| 0.06×0.183 |
| 时间/min 浓度/mol.L |
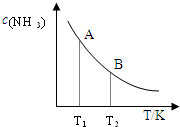
c (N2) | c (H2) | c (NH3) |
| 0 | 0.6 | 1.8 | 0 |
| 3 | 0.52 | x | 0.16 |
| 6 | 0.36 | 1.08 | 0.48 |
| 9 | 0.36 | 1.08 | 0.48 |
查看答案和解析>>
科目:高中化学 来源: 题型:
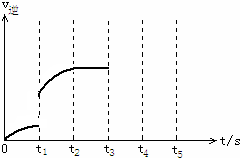 可逆反应Fe(s)+CO2(g)?FeO(s)+CO(g),在温度938K时,平衡常数K=1.47,在1173K时,K=2.15
可逆反应Fe(s)+CO2(g)?FeO(s)+CO(g),在温度938K时,平衡常数K=1.47,在1173K时,K=2.15| C(CO) |
| C(CO2) |
| C(CO) |
| C(CO2) |
查看答案和解析>>
科目:高中化学 来源:同步题 题型:不定项选择题
 3C(g)+D(g)达平衡时,C的浓度为Wmol/L。若维持容器体积和温度不变,按下列四种配比作为起始物质,达平衡后,C的浓度仍为Wmol/L的是
3C(g)+D(g)达平衡时,C的浓度为Wmol/L。若维持容器体积和温度不变,按下列四种配比作为起始物质,达平衡后,C的浓度仍为Wmol/L的是 [ ]
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com