
【题目】按要求作答
(1)钴位于元素周期表的第__族,其基态原子中未成对电子个数为__。
(2)[Fe(H2NCONH2)6](NO3)3的名称是三硝酸六尿素合铁(Ⅲ),是一种重要的配合物。该化合物中Fe3+的核外电子排布式为__,所含非金属元素的电负性由大到小的顺序是__。
(3)尿素[CO(NH2)2]分子中σ键与π键的数目之比为__。
(4)硒、硅均能与氢气化合形成气态氢化物,若“Si-H”中共用电子对偏向氢,氢气与硒反应时,硒单质做氧化剂,则硒与硅的电负性大小为Se__Si(填“>”或“<”)
(5)与Si同周期部分元素的逐级电离能如图所示,其中a、b和c分别代表__。
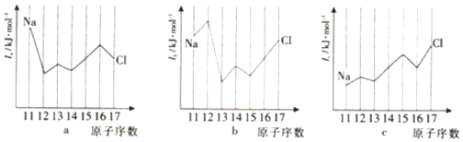
A.a为I1、b为I2、c为I3 B.a为I2、b为I3、c为I1
C.a为I3、b为I2、c为I1 D.a为I1、b为I3、c为I2
【答案】VIII 3 [Ar]3d5或1s22s22p63s23p63d5 O>N>C>H 7:1 > B
【解析】
(1)钴为27号元素,位于第四周期VIII族,其价电子排布式为3d74s2;
(2)Fe的价电子排布式为3d64s2,则Fe3+的核外电子排布式为[Ar]3d5;所含非金属元素为H、C、N、O;
(3)尿素[CO(NH2)2]的结构简式为![]() ;
;
(4)“Si-H”中共用电子对偏向氢,则Si为正价,氢气与硒反应时,硒单质做氧化剂,则硒化合价降低,为负价,则硒的电负性大于硅的;
(5)图像a,Na的电离能最大,此时的含Na元素的微粒处于稳定结构,则为第二电离能;图像b中含Mg微粒的电离能最大,则含Mg微粒处于稳定结构,为第三电离能;图像c与第一电离能相同,则为第一电离能。
(1)钴为27号元素,位于第四周期VIII族,其价电子排布式为3d74s2,未成对电子个数为3;
(2)Fe的价电子排布式为3d64s2,则Fe3+的核外电子排布式为[Ar]3d5或1s22s22p63s23p63d5;所含非金属元素为H、C、N、O,电负性由大到小的顺序是O>N>C>H;
(3)尿素[CO(NH2)2]的结构简式为![]() ,含有7条σ键,1条π键,比值为7:1;
,含有7条σ键,1条π键,比值为7:1;
(4)“Si-H”中共用电子对偏向氢,则Si为正价,氢气与硒反应时,硒单质做氧化剂,则硒化合价降低,为负价,则硒的电负性大于硅的;
(5)图像a,Na的电离能最大,此时的含Na元素的微粒处于稳定结构,则为第二电离能;图像b中含Mg微粒的电离能最大,则含Mg微粒处于稳定结构,为第三电离能;图像c与第一电离能相同,则为第一电离能,答案为B。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】如图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。下列有关说法正确的是( )
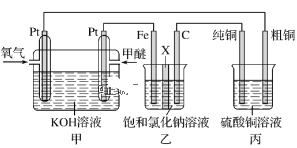
A.反应一段时间后,乙装置中生成的氢氧化钠在铁极区
B.乙装置中铁电极为阴极,电极反应式为Fe-2e-=Fe2+
C.甲中通入氧气的一极为阳极,发生的电极反应为O2+4e-+2H2O=4OH-
D.反应一段时间后,丙装置中硫酸铜溶液浓度保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下超氧化钾晶体呈立方体结构,晶体中氧的化合价部分为0价,部分为﹣2价.如图所示为超氧化钾晶体的一个晶胞(晶体中最小的重复单元),则下列说法中正确的是

A. 晶体中每个K+周围有8个O2﹣,每个O2﹣周围有8个K+
B. 晶体中与每个K+距离最近的K+有8个
C. 超氧化钾的化学式为KO2,每个晶胞含有4个K+和4个O2﹣
D. 晶体中,0价氧与﹣2价氧的数目比为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把图二的碎纸片补充到图一中,可得到一个完整的离子方程式。对该离子方程式说法正确的是
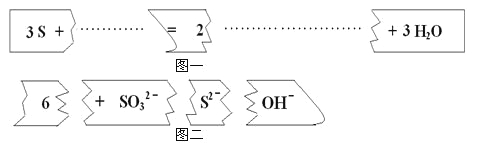
A. 配平后的化学计量数依次为3、1、2、6、3
B. 若有1mol的S被氧化,则生成2mol S2-
C. 氧化剂与还原剂的物质的量之比为1:2
D. 2mol的S参加反应有3mol的电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某高分子材料的结构如图所示:已知该高分子材料是由三种单体聚合而成的,以下与此高分子材料相关的说法正确的是( )

A.三种单体中有两种有机物互为同系物
B.三种单体都可以使溴水褪色,但只有两种能使酸性高锰酸钾溶液褪色
C.形成该高分子材料的单体![]() 中,所有原子一定处于同一平面
中,所有原子一定处于同一平面
D.该高分子材料是体型高分子,合成它的反应是加聚反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(I)![]() 和
和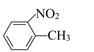 的一些物理性质如下表:
的一些物理性质如下表:
物质 | 熔点 | 沸点 | 密度 | 水溶性 |
| -10℃ | 212℃ | 1.1622g/mL | 不溶于水 |
| 54℃ | 238℃ | 1.1581g/mL | 不溶于水 |
①分离这两种物质混合物可采用的方法是__。(填序号)
A.过滤 B.分液 C.蒸发 D.分馏
②实验需要用到的主要玻璃仪器是___。
(II)酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、粘合剂及印刷、纺织等工业。乙酸乙酯的实验室和工业制法常采用如下反应:CH3COOH+C2H5OH![]() CH3COOC2H5+H2O
CH3COOC2H5+H2O
请根据要求回答下列问题:
(1)欲提高乙酸的转化率,可采取的措施有___、___等。
(2)若用如图所示装置来制备少量的乙酸乙酯,产率往往偏低,其原因可能为___、___。
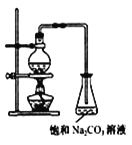
(3)此反应以浓硫酸为催化剂,可能会造成___、__问题。
(4)目前对该反应的催化剂进行了新的探索,初步表明质子酸离子液体可用作反应的催化剂,且能重复使用。实验数据如下表所示(乙酸和乙醇以等物质的量混合)
同一反应时间 | 同一反应温度 | ||||
反应温度/℃ | 转化率(%) | 选择性(%) | 反应时间/h | 转化率(%) | 选择性(%) |
40 | 77.8 | 100 | 2 | 80.2 | 100 |
60 | 92.3 | 100 | 3 | 87.8 | 100 |
80 | 92.6 | 100 | 4 | 92.3 | 100 |
120 | 94.5 | 98.7 | 6 | 93.0 | 100 |
选择性100%表示反应生成的产物是乙酸乙酯和水 | |||||
根据表中数据,下列___(填字母)为该反应的最佳条件。
A.120℃,4h B.80℃,2h
C.60℃,4h D.40℃,3h
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.已知将盐酸滴入高锰酸钾溶液中,产生黄绿色气体,而溶液的紫红色褪去。现有一个氧化还原反应的体系中共有KCl、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 七种物质:
七种物质:
(1)写出一个包含上述七种物质的氧化还原反应方程式:____________。
(2)上述反应中,1mol氧化剂在反应中得到________mol电子。
(3)如果在反应后的溶液中加入![]() ,溶液又变紫红色。已知铋有
,溶液又变紫红色。已知铋有![]() 、
、![]() 价,其中
价,其中![]() 价较稳定,写出加入
价较稳定,写出加入![]() 溶液又变紫红色的离子方程式:_________。由上述方程式说明
溶液又变紫红色的离子方程式:_________。由上述方程式说明![]() 的一个性质:__________。
的一个性质:__________。
II.(1)已知![]() 能与次氯酸盐发生如下反应(未配平)
能与次氯酸盐发生如下反应(未配平)![]() 。
。
①已知有10.7gFe(OH)3参加反应,共转移了![]() 个电子,则
个电子,则![]() ________。
________。
②根据所学的知识,推测![]() 能和下列________
能和下列________![]() 填序号
填序号![]() 物质反应。
物质反应。
A.![]() B.SO2 C.
B.SO2 C.![]() D.
D.![]()
(2)一定条件下,向含硝酸的废水中加入![]() ,将
,将![]() 还原成
还原成![]() 。若该反应消耗32gCH3OH,转移6mol电子,则参加反应的还原剂和氧化剂的物质的量之比是________。
。若该反应消耗32gCH3OH,转移6mol电子,则参加反应的还原剂和氧化剂的物质的量之比是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 和
和![]() 六种粒子,属于同一氧化还原反应中的反应物和生成物,下列叙述不正确的是
六种粒子,属于同一氧化还原反应中的反应物和生成物,下列叙述不正确的是
A.被氧化和被还原的离子数目比为![]()
B.该反应说明![]() 、
、![]() 、、
、、![]() 在溶液不能大量共存
在溶液不能大量共存
C.每![]() 发生氧化反应,转移
发生氧化反应,转移![]()
D.若利用该反应设计原电池,则负极反应为:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是
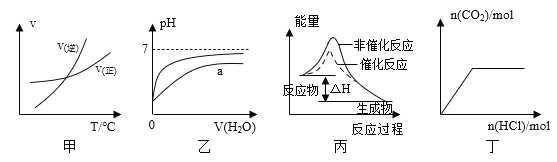
A. 由图甲表示的反应速率随温度变化的关系可知该反应的ΔH>0
B. 图乙表示pH相同的盐酸与醋酸中分别加入水后溶液pH的变化,其中曲线a对应的是醋酸
C. 图丙表示该反应为放热反应,且催化剂能改变反应的焓变
D. 图丁表示向Na2CO3溶液中逐滴滴加稀盐酸,生成CO2与所加盐酸物质的量的关系
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com