
| A. | H2、NaOH | B. | H2、Al(OH)3 | C. | H2、NaCl、NaAlO2 | D. | H2、NaCl、Al(OH)3 |
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等质量的乙酸、葡萄糖与淀粉完全燃烧时消耗氧气的质量相等 | |
| B. | 按系统命名法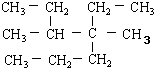 的名称为4,5-二甲基-4-乙基庚烷 的名称为4,5-二甲基-4-乙基庚烷 | |
| C. | 豆浆中富含大豆蛋白,煮沸后蛋白质水解成了氨基酸 | |
| D. | 某烯烃(最简式为CH2)与H2加成产物为2,3-二甲基丁烷,则该烯烃可能有2种结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol醋酸的质量与NA个醋酸分子的质量相等 | |
| B. | NA个氧分子和NA个氢分子的质量比为16:1 | |
| C. | 28g氮气所含原子数目为NA | |
| D. | 在标准状况下,0.5NA个氯气分子所占的体积约是11.2L |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
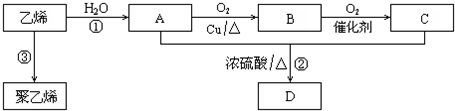
 ;反应类型:加聚反应
;反应类型:加聚反应查看答案和解析>>
科目:高中化学 来源: 题型:填空题
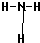 .氨常作致冷剂,是因为氨气具有氨气易液化,挥发后吸收能量使周围温度降低的性质.氨气溶于水得到氨水,氨水显碱性的原因是(用电离方程式表示)NH3•H2O?NH4++OH-.玻璃棒蘸浓盐酸接触氨气时,观察到的现象为冒白烟.
.氨常作致冷剂,是因为氨气具有氨气易液化,挥发后吸收能量使周围温度降低的性质.氨气溶于水得到氨水,氨水显碱性的原因是(用电离方程式表示)NH3•H2O?NH4++OH-.玻璃棒蘸浓盐酸接触氨气时,观察到的现象为冒白烟.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
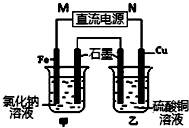 如图装置中甲烧杯盛放100mL 0.2mol/L 的NaCl溶液,乙烧杯盛放100mL 0.5mol/L的CuSO4溶液.反应一段时间后,停止通电.向甲烧杯中滴入几滴酚酞,观察到石墨电极附近首先变红,通电一段时间后(溶液中还有CuSO4),若要使乙烧杯中电解质溶液恢复到电解前的状态,可加入AC (填序号).
如图装置中甲烧杯盛放100mL 0.2mol/L 的NaCl溶液,乙烧杯盛放100mL 0.5mol/L的CuSO4溶液.反应一段时间后,停止通电.向甲烧杯中滴入几滴酚酞,观察到石墨电极附近首先变红,通电一段时间后(溶液中还有CuSO4),若要使乙烧杯中电解质溶液恢复到电解前的状态,可加入AC (填序号).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com